의사
의사
채용
NGS 기반 HLA 정밀진단 검사제품 유럽 CE 허가
엔젠바이오, 골수 및 장기이식 위한 '조직 적합성 검사' 사용
[데일리메디 한해진 기자] NGS 정밀진단 플랫폼 전문기업 엔젠바이오(대표이사 최대출)가 차세대염기서열분석 (NGS) 기반 진단 제품 ‘HLAaccuTest™ All’에 대한 유럽 체외진단 의료기기 인증(CE-IVD)을 획득했다고 23일 밝혔다.
HLA(Human Leukocyte Antigen, 인간백혈구항원) 검사란 장기와 조혈모세포 이식 시 공여자와 수여자의 조직 적합성 일치 여부를 검증하는 것으로 이식 부작용을 최소화하기 위해 필수적으로 시행한다.
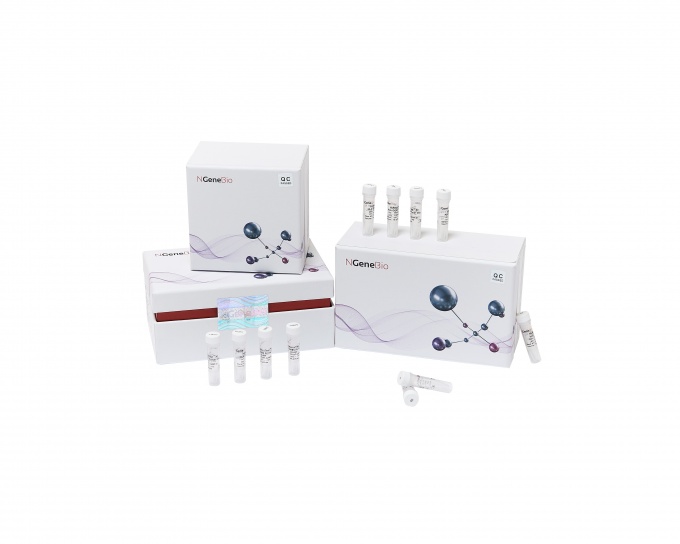
엔젠바이오에 따르면 HLAaccuTest™ All은 HLA 유전자 좌위 11종(HLA-A, B, C, DRB1/3/4/5, DQB1, DPB1, DQA1, DPA1)을 한 번에 NGS 검사할 수 있는 유일한 국내 제품이다. 이는 골수 또는 장기이식을 위한 조직 적합성 검사에 사용된다.
엔젠바이오가 이번에 인증받은 CE-IVD는 품질 적합성을 증명해서 의무적으로 획득해야 하는 인증으로 모든 체외진단 의료기기가 유럽 시장에서 시판과 유통을 진행하는데 필수적이다.
특히 체외진단 의료기기 중 HLA 검사 제품은 이식수술 안전성을 담보하기 때문에 다른 일반 체외진단의료기기보다 높은 수준의 인증심사 기준 충족을 요구하고 있다.
이에 회사는 최고 수준의 독일 인증기관인 TÜV SÜD로부터 약 1년간 제품 성능과 품질을 검증받아 인증을 취득했다.
엔젠바이오는 지난 5월 식품의약품안전처로부터 HLA 유전자 좌위 5종을 동시에 정확히 검사할 수 있는 NGS 진단제품 ’HLAaccuTest™’를 허가 받은 바 있다.
회사 관계자는 “NGS 기반 HLA 진단 제품은 패널 디자인과 실험 조건을 최적화해 기존 HLA 검사 기술의 한계점인 판독 모호성을 크게 향상시킨 제품”이라며 “이번에 CE-IVD 인증을 취득한 제품은 좀 더 많은 좌위를 검사할 수 있어 해외서도 경쟁력이 높다”고 전했다.