뉴스 - 제약‧바이오

도네페질·아세틸카르티닌 성분 함유 '치매약' 타격
식약처, 임상재평가 결과 분석···'혈관성 치매 증상 개선 적응증 삭제'
박정연 기자 (dailymedi@dailymedi.com)
2019.05.10 16:48
이에 따라 삭제된 적응증 관련 처방과 조제는 곧바로 중단된다. 해당 적응증에 대한 허가사항은 오는 7월 취소된다.
식품의약품안전처는 '도네페질'과 '아세틸엘카르니틴'에 대한 임상재평가 결과를 종합해 일부 적응증을 삭제한다는 내용의 의약품 안전성 서한을 9일 배포했다.
앞서 식약처는 도네페질과 아세틸엘카르니틴과 제제에 대한 재검증이 필요하다고 판단해 임상재평가를 진행했다.
임상재평가 후 업체들은 해당 치료제가 가진 적응증에 대한 임상시험 결과를 제출했다. 그러나 식약처 검토 결과, 일부 효능·효과에 대한 유효성을 입증하지 못한 것으로 평가됐다.
이에 따라 도네페질의 기허가 내용 중 '혈관성 치매 증상 개선(뇌혈관 질환을 동반한 치매)'은 적응증에서 삭제된다.
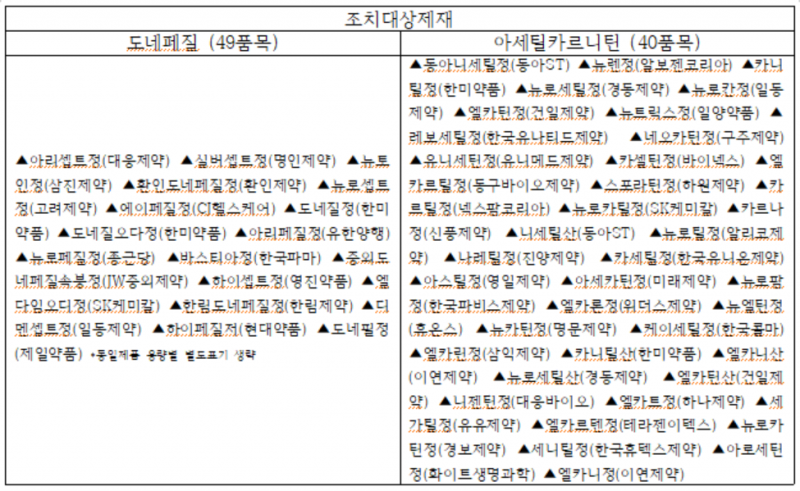
알츠하이머형 치매 증상의 치료에 대한 유용성은 유효한 것으로 인정된다. 이번 조치 대상은 제재에는 명인제약 실버세트정, 영진약품 하이셉트정 등 20개사 49품목이다.
아세틸엘카르니틴의 경우 '일차적 퇴행성 질환'이 적응증에서 삭제된다.
'이차적 퇴행성 질환'의 경우엔 적응증이 유효하다. 다만 오는 2021년 1월 25일까지 효능 및 효과에 대한 임상재평가가 진행될 예정이다. 조치 대상은 한미약품 카니틸정, 경동제약 뉴로세틸정 등 등 35개사 40품목이다.
저작권자 © 데일리메디 무단전재및 재배포 금지
 박정연 기자 (
박정연 기자 (