뉴스 - 행정/법률

서울대·세브란스·아산 등 참여 '중앙IRB' 정식 출범
식약처, 40개병원 협력 임상시험 통합 심사···'공적 필요성 큰 의약품 대상'
양보혜 기자 (bohe@dailymedi.com)
2021.07.30 15:02
[데일리메디 양보혜 기자] 코로나19 백신과 치료제 등의 신속한 임상시험 진입을 지원하는 중앙임상시험심사위원회(이하 중앙IRB, Institutional Review Board)가 정식 출범한다.
식품의약품안전처(처장 김강립)는 중앙IRB 출범을 알리고 주요 참여 병원의 적극적인 협조를 구하기 위해 30일 서울아산병원에서 출범식을 개최한다고 밝혔다.
이번 출범식에서는 중앙IRB 협약병원 관계자와 심사위원들에게 ▲제도 도입 취지 ▲추진 경과 ▲운영계획 등을 소개하고, 제도의 원활한 정착을 위한 제언을 청취했다.
중앙IRB 제도는 대규모 다기관 임상시험 시 기관별 IRB에서 각각 심사하지 않고 중앙IRB에서 한번에 통합 심사하는 제도다.
또한 참여기관의 심사 효율성과 신뢰성을 높이기 위해 개별 기관의 IRB 위원이 참여하는 공동심사위원회 형태로 운영할 계획이다.
코로나19 치료제·백신, 항암제 등 공적 필요성이 큰 의약품의 임상시험을 시작으로 심사대상을 점차 확대할 예정이다.
김강립 식약처장은 이번 출범식에서 “중앙임상시험심사위원회의 출범이 규제과학을 바탕으로 한 국내 임상시험 심사 전문성을 강화하는 밑바탕이 되길 바란다”고 말했다.
이어 “식약처는 코로나19 백신과 치료제 등의 신속한 개발을 위해 가능한 모든 지원을 아끼지 않을 것”이라며 “임상시험 수행 기관과 심사위원들도 중앙임상시험심사위원회에 대한 적극적인 관심과 참여를 바란다”고 당부했다.
식품의약품안전처(처장 김강립)는 중앙IRB 출범을 알리고 주요 참여 병원의 적극적인 협조를 구하기 위해 30일 서울아산병원에서 출범식을 개최한다고 밝혔다.
이번 출범식에서는 중앙IRB 협약병원 관계자와 심사위원들에게 ▲제도 도입 취지 ▲추진 경과 ▲운영계획 등을 소개하고, 제도의 원활한 정착을 위한 제언을 청취했다.
중앙IRB 제도는 대규모 다기관 임상시험 시 기관별 IRB에서 각각 심사하지 않고 중앙IRB에서 한번에 통합 심사하는 제도다.
이번 중앙IRB 출범으로 여러 병원에서 실시하는 ‘다기관 임상시험’을 통합 심사할 수 있는 체계가 마련되면 병원마다 각각의 임상시험 계획을 심사했던 행정절차의 중복과 임상시험 승인까지 소요되는 기간이 단축돼 신속한 임상시험 진입이 가능해진다.
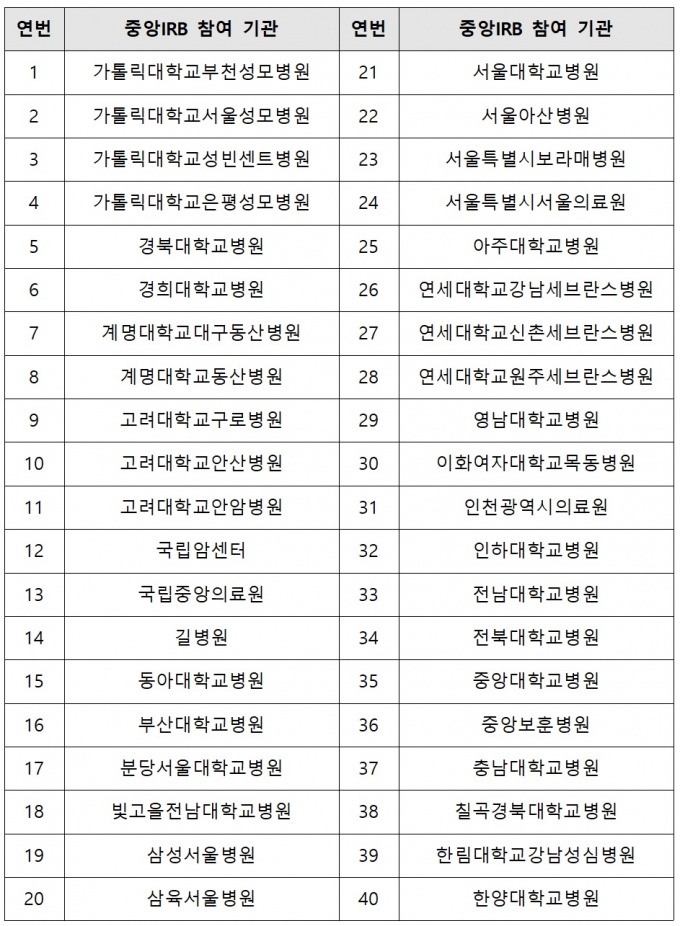
중앙IRB에는 코로나19 백신 등 임상시험 수행 기관, 임상시험 수행 상위 기관 등 총 40개 병원[표]이 참여할 예정이다.
40개 병원에는 서울대병원, 세브란스병원, 가톨릭대 서울성모병원, 삼성서울병원, 서울아산병원, 국립암센터 등이 포함된다.
40개 병원에는 서울대병원, 세브란스병원, 가톨릭대 서울성모병원, 삼성서울병원, 서울아산병원, 국립암센터 등이 포함된다.
또한 참여기관의 심사 효율성과 신뢰성을 높이기 위해 개별 기관의 IRB 위원이 참여하는 공동심사위원회 형태로 운영할 계획이다.
코로나19 치료제·백신, 항암제 등 공적 필요성이 큰 의약품의 임상시험을 시작으로 심사대상을 점차 확대할 예정이다.
김강립 식약처장은 이번 출범식에서 “중앙임상시험심사위원회의 출범이 규제과학을 바탕으로 한 국내 임상시험 심사 전문성을 강화하는 밑바탕이 되길 바란다”고 말했다.

저작권자 © 데일리메디 무단전재및 재배포 금지
 양보혜 기자 (
양보혜 기자 (