뉴스 - 제약‧바이오

국내 코로나19 치료제 특허 출원 활발 총 '302건'
특허청 '화합물 100건·항체의약품 69건·천연물 69건 등'
임수민 기자 (min0426@dailymedi.com)
2021.08.14 06:10
[데일리메디 임수민 기자] 코로나19 장기화에 세계 각국이 게임 체인저로 떠오를 치료제 개발에 심혈을 기울이는 가운데 국내에서도 제약사와 연구소들이 치료제 개발에 속도를 내며 관련 특허 출원이 이어지고 있다.
특히 코로나19 치료제 특허 출원은 지난 2월 국내 최초로 렉키로나주가 정맥주사제로 조건부 허가를 받은 이후 더욱 활기를 띠는 모양새다.
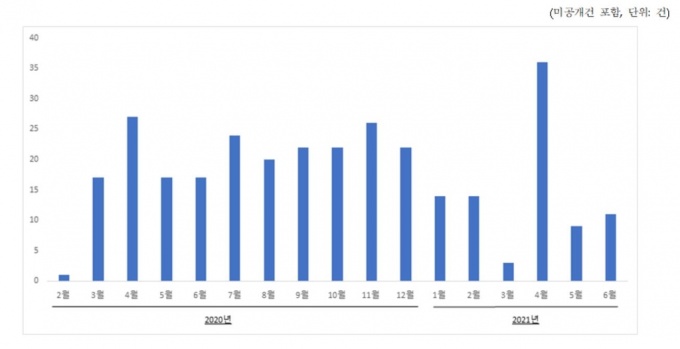
13일 특허청에 따르면 코로나19 치료제 관련 특허는 발병 초기인 지난해 2월부터 꾸준히 출원돼 금년 6월까지 모두 302건에 달했다. 이 가운데 현재 코로나19에 대한 항바이러스 효과로 특허 등록된 출원은 총 13건이다.
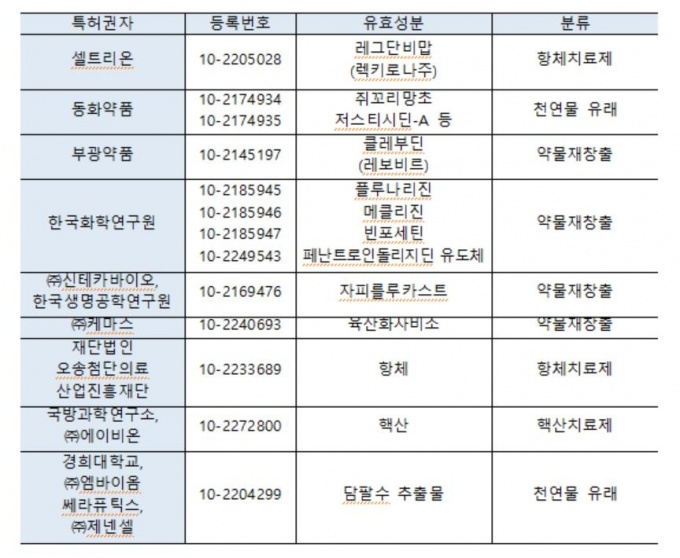
코로나19 치료제로 허가받은 특허는 셀트리온 '렉키로나주'(레그단비맙, 항체치료제) 1건이다.
동화약품 'DW2008S'(쥐꼬리망초 유래 신약)는 특허 2건이 등록돼 임상을 진행 중이며, 부광약품 '레보비르'(클레부딘, 약물 재창출)는 임상이 종료됐다.
출원인별로는 국내 제약사 등 기업이 147건, 정부 기관 및 출연연구소 66건, 대학 55건, 개인 30건, 외국인 4건 순이다.
외국인 특허는 국제출원 후 31개월 내 국내 출원하면 되는 만큼 대부분 아직 국내 단계에 진입하지 않은 상황으로 추정된다.
국내 출원된 코로나19 치료제는 유효성분에 따라 화합물, 항체의약품, 천연물 등으로 나뉜다. 각각 100건, 69건, 69건의 특허가 출원됐다.
제약사들은 신약 뿐 아니라 단기간 내 치료제를 개발하기 위해 기존 의약품을 활용한 약물 재창출 방식 등 다양한 시도를 하는 것으로 분석된다.
국가 연구개발사업을 기반으로 출원된 건이 전체(302건)의 25.8%(78건)를 차지했다. 일반적으로 국가 연구개발사업에 따른 특허 출원은 전체 출원의 15% 미만이다.
글로벌 제약사들도 코로나19 치료제 개발에 한창이다.
미국 식품의약국(FDA)은 일라이 릴리, 리제네론, 제넨텍, GSK의 정맥주사제와 길리아드의 렘데시비르 등 총 11개 치료제에 대해 긴급사용을 승인했고, 그중 렘데시비르만 정식으로 허가했다.
미국 머크(MSD)사는 경구용 치료제 몰누피라비르 개발에 집중하고 있고, 임상시험 결과에 따라 연내 FDA 긴급사용승인도 이뤄질 것으로 예상된다. 타미플루를 개발했던 로슈와 화이자도 경구용 코로나 치료제로 임상을 진행하고 있다.
특허청 약품화학심사과 곽희찬 심사관은 "특허발명을 의약품으로 사용하려면, 추가적인 기술개발이 필요할 수 있고 임상시험 결과에 기초한 안전성 및 유효성 심사를 거쳐 식품의약품안전처 허가를 받아야 한다"며 "의약품은 특허를 등록받았다고 해서 바로 사용할 수 있는 것은 아니며, 꼼꼼한 사후 절차가 있음을 유의해야 한다"고 강조했다.
저작권자 © 데일리메디 무단전재및 재배포 금지
 임수민 기자 (
임수민 기자 (