
 삼성바이오에피스(대표 고한승)가 황반변성 치료제 바이오시밀러의 서울아산병원 진입을 시도했으나 고배를 마신 것으로 확인됐다.
삼성바이오에피스(대표 고한승)가 황반변성 치료제 바이오시밀러의 서울아산병원 진입을 시도했으나 고배를 마신 것으로 확인됐다.
서울아산병원의 상징성 등 향후 경쟁제품 보유 제약사인 종근당과 대형병원 처방권 진입을 두고 경쟁이 가열될 전망이다.
다른 성분으로 황반변성 치료제 바이오시밀러인 아일리아를 품목허가 준비 중인 셀트리온 행보도 주목된다.
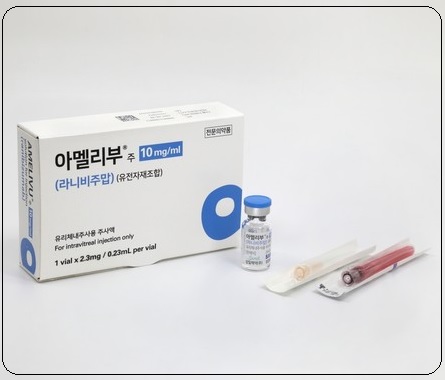
8일 업계에 따르면 서울아산병원 약사위원회(DC)는 최근 신규약물심사 과정에서 삼성바이오에피스 황반변성 치료제 바이오시밀러 ‘아멜리부’를 허가하지 않기로 결정했다. 회사 측이 적잖은 공을 들였는데 탈락한 것이다.
제넨텍(현 로슈) 황반변성 치료제 루센티스가 오리지널 바이오의약품이다. 국내에서는 삼성바이오에피스와 종근당이 각각 아멜리부, 루센비에스라는 이름으로 바이오시밀러 제품을 출시했다.
특히 금년 1월부터 삼성바이오에피스 아멜리부, 종근당 루센비에스 두 품목이 급여 등재되면서 양사간 경쟁이 치열해지고 있는 상황이다.
종근당 루센비에스는 가격과 제형에서 강점이 있다. 루센비에스 가격은 30만원으로 오리지널 58만원 대비 크게 낮췄다. 여기에 루센티스 시밀러 중 유일하게 프리필드시린지 제형으로 품목허가도 받았다.
경쟁 제품인 삼성바이오에피스 아멜리부는 당초 글로벌 임상 규모 등 데이터를 강점으로 내세웠으나, 급여 등재 2개월 만에 46만원에서 35만원까지 가격을 낮춘 바 있다.
하지만 서울아산병원이 두 품목을 처방 약물에 포함하지 않으면서 대형병원 진입이 다소 난항을 겪는 모습이다.
서울아산병원은 DC 심사 과정에서 신규통과약물로 지정하는 것을 고심했으나 이번에는 통과시키지 않았다. 구체적인 사유는 알리지 않았다.
서울아산병원 DC 탈락과 관련, 삼성바이오에피스 관계자는 "국내 유통 및 판매권은 삼일제약이 담당 하고 있어 우리는 알지 못하는 상황"이라고 말했다. 삼일제약 관계자도 "관련 내용에 대해 확인 중"이라고 짧은 입장을 전했다.
종근당 관계자는 "루센비에스는 이번에 서울아산병원 DC 심사 신청을 하지 않았다"며 "프리필드시린지 제형을 통해 추후 신청 계획이나 정해진 것은 없다"고 말했다.
제약사들은 신약 출시 이후 대형병원 처방권 진입을 위해 처방 심의를 통과해야 한다. ‘드럭 커미티(DC, drug committee)’라고 불리우는 병원 약물심사위원회를 거친 후 처방이 가능하다.
서울아산병원 등 소위 빅5로 불리우는 병원들의 처방권 진입은 시장 영향력을 확대하는 큰 관문 중 하나다. DC 결과에 따라 제품 시장 점유율을 예측할 수 있는 바로미터가 되기 때문이다.
결과적으로 서울아산병원 DC 탈락이 업체들에겐 큰 아픔이 될 수 있다. 특히 서울아산병원의 경우 황반변성 치료제 시밀러를 통과시키지 않은 만큼 내년에 선보일 다른 성분의 바이오시밀러 제품도 낙관하기 어려울 전망이다.
현재 삼성바이오에피스와 셀트리온은 황반변성 치료제 ‘아일리아’ 바이오시밀러를 준비하고 있는 상태다. 이 제품도 국내 품목허가 이후 서울아산병원 DC 통과가 수월하지 않을 수 있다.
서울아산병원 관계자는 "관련 내용들은 현재 따로 공식화 된 것은 없다"면서 "제약사들이 얽힌 문제여서 탈락 사유 및 통과 여부 내용 등을 공개하기 어렵다"고 조심스러운 입장을 전했다.
 최진호 기자 (
최진호 기자 (