[데일리메디 양보혜 기자] 미국 식품의약국(FDA)이 유전자치료제 개발의 나침반이라고 할 수 있는 '가이드라인'을 발표함에 따라 향후 국내외 기업들의 유전자치료제 개발이 탄력을 받을 것으로 전망된다.
19일 업계에 따르면 최근 FDA는 성장잠재력이 높은 유전자치료제 시장의 지속적인 발전을 위한 정책적 기틀을 마련하고자 관련 가이드라인 초안을 마련했다고 밝혔다.
글로벌 유전자치료제 시장은 2018년 1억4400만달러(약 1628억원) 규모에서 연평균 108% 성장, 2024년에는 약 115억 달러(약 13조원) 규모에 이를 것으로 예측된다.
FDA 스콜 고틀립(Scott Gottleib) 국장은 “혈우병, 망막장애, 희귀질환 등에 대한 개발 지침뿐만 아니라 생산 및 장기투여 안전성에 관한 내용이 담겨 있는 총 6가지 세부 가이드라인을 만들었다”고 설명했다.
구체적으로 보면 특정질환 개발에 관한 지침이 3개, 생산 관련 내용이 3개로 구성돼 있다.
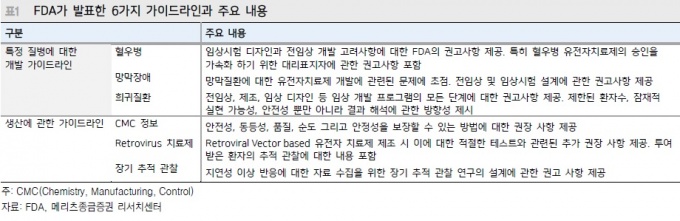
우선, 혈우병, 망막장애, 희귀질환 등 특정질환에 관한 전임상, 임상 디자인 시 고려사항에 대한 내용이 공통적으로 포함됐다.
혈우병의 경우 유전자치료제의 승인을 가속화하기 위한 대리표지자에 관한 권고안이 새로 마련됐으며, 희귀질환은 제안된 환자 수, 잠재적 실현가능성, 안전성은 물론 결과 해석에 관한 방향성도 제시됐다.
지금까지 별다른 지침이 없었던 유전자치료제 생산에 관한 지침도 처음 공개됐다. 제조공정 및 품질(CMC) 정보, 레트로바이러스(Retrovirus)치료제, 장기 추적 관찰 시 고려사항 등이 세부적으로 담겼다.
CMC정보의 경우 유전자치료제의 안전성, 동등성, 품질, 순도 그리고 안정성을 보장할 수 있는 방법에 대한 권고사항이 제시됐다.
 양보혜 기자
양보혜 기자