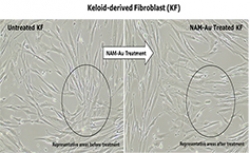
임상시험 부담 완화 기대 속 '안전성·유효성' 검증 기준 논란 제기
미국 식품의약국(FDA)이 신약 허가 시 요구해온 확증 임상시험 기준을 완화하는 방향을 예고하면서 글로벌 의약품 개발 환경에 변화가 예상된다.23일 업계에 따르면 FDA는 신약 승인 과정에서 통상적으로 요구해온 최소 2건의 확증 임상시험 요건을 1건으로 축소하는 방안을 검토 중인 것으로 전해졌다그간 FDA는 통계적으로 독립된 두 건 이상의 적절하고 충분히 통제된 임상시험(adequate and well-controlled trials)을 통해 유효성과 안전성을 입증하도록 요구해왔다. 이는 신약 허가의 ‘골든 스탠더드’로 받아들…
2026-02-23 11:49:28