
아스트라제네카 항암제 타그리소(성분명 오시머티닙)가 폐암 1차 치료제로서 급여 적정성을 인정받으며 급여화를 위한 본격적인 행보를 시작했다.
지난 3월 타그리소는 'EGFR 엑손 19 결손 또는 엑손 21(L858R) 치환 변이된 국소 진행성 또는 전이성 비소세포폐암 환자의 1차 치료'로 급여기준이 설정된 바 있다.
또 신경섬유종 치료제 ‘코셀루고’ 등 3개 약제가 약평위를 통과하면서 급여화에 한발짝 다가섰다. 코셀루고는 한국희귀·난치성질환연합회가 신속한 보험급여를 촉구하는 진정서를 제출하는 등 대중적 관심이 높은 약제다.
7일 건강보험심사평가원은 ‘2023년 제10차 약제급여평가위원회’를 통해 7개 약제에 대한 심의결과를 공개했다.
이번 약평위에서는 3개 약제가 급여적정성을 인정받았으며 2개 약제는 조건부 급여인정, 1개 약제는 비급여로 결정됐다.
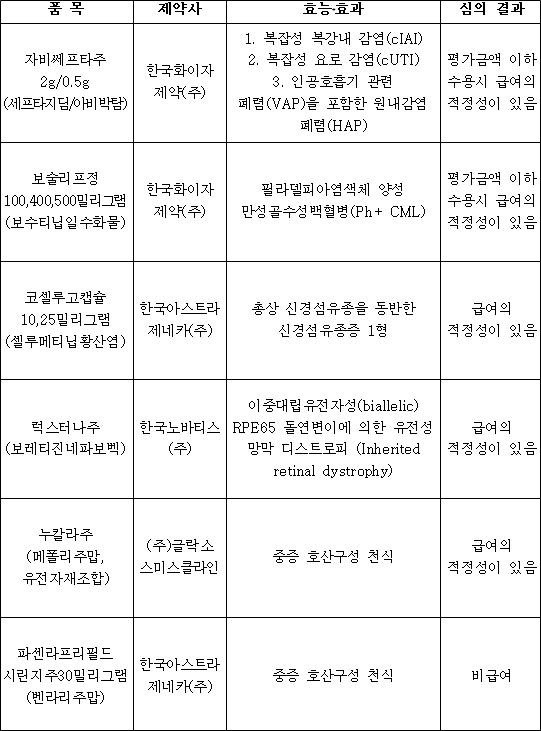
약평위 통과 약제를 보면, 우선 한국아스트라제네카의 ‘코셀루고캡슐(성분: 셀루메티닙황산염)’ 10mg, 25mg가 총상 신경섬유종을 동반한 신경섬유종증 1형에 대한 급여 적정성을 인정받았다.
지난 2021년 5월 식품의약품안전처로부터 신속심사제도 1호로 선정돼 국내 허가를 받았으나, 지난해 3월 약평위에서 비급여로 탈락했다. 재심의에서 급여적정성을 다시금 인정받은 것이다
또 한국노바티스 ‘럭스터나주(성분: 보레티진네파보벡)’는 이중대립유전자성(biallelic) RPE65 돌연변이에 의한 유전성 망막 디스트로피(Inherited retinal dystrophy)에 대한 치료로, GSK의 ‘누칼라주(성분: 메폴리주맙)’는 중증 호산구성 천식 치료로 각각 급여 적정성을 인정받았다.
반면 누칼라주와 같은 중증 호산구성 천식으로 신청한 한국아스트라제네카의 ‘파센라프리필드시린지주 30mg(성분: 벤라리주맙)’은 비급여로 탈락했다.
조건부 급여인정 약제는 한국화이자의 ‘자비쎄프타주 2g/0.5g(성분: 세프타지딤/아비박탐)’과 ‘보술리프정(성분: 보수티닙일수화물)’ 100mg, 400mg, 500mg 2개 품목이다.
자비쎄프타주는 ▲복잡성 복강내 감염(cIAI) ▲복잡성 요로 감염(cUTI) ▲인공호흡기 관련 폐렴(VAP)을 포함한 원내감염 폐렴(HAP) 등 3개 치료 효능효과로, 보술리프는 필라델피아염색체 양성 만성골수성백혈병(Ph+ CML)에 대한 치료 효능효과로 평가금액 이하 수용 시 급여적정성이 있다고 인정됐다.
이번에 약평위를 통과한 약제들은 국민건강보험공단과의 약가협상을 거쳐 건강보험정책심의위원회(건정심)에 상정, 의결되면 최종적으로 보험급여를 적용받게 된다.
