식약처, 코로나19 극복 적극행정 나서
의약품 허가·임상, 필수의약품 공급 등 각종 지원책 마련
[데일리메디 양보혜 기자] 식품의약품안전처(처장 이의경)는 환자 치료기회를 보장하고 제약업계 부담을 덜어주기 위한 코로나19 위기 극복 방안으로 의약품 분야에서 과감한 적극행정을 추진 중이다.
총 6가지 지원책이 마련됐는데, △국가필수의약품의 차질 없는 공급 △허가신청절차 간소화 △코로나19 임상시험 의료기관 확대 △비임상시험자료, 해외 실태조사를 서류평가로 완화, 제약업체 교육이수 의무기한 연장, BSE 미감염 증명 제출자료 요건 완화 등이다.
우선, 대체약이 없어 수입에만 의존하는 국가필수의약품은 국내 품질검사를 일부 생략하고 해외 제조원의 시험성적서를 인정함으로써 환자들에게 원활히 공급될 수 있도록 지원하고 있다.
의약품 허가 신청서류 중 코로나19로 제출하기 어려운 서류에 대해서는 공증 받아 제출해야 하는 원본서류 대신 원본과 동일함을 확인할 수 있는 전자문서를 제출할 수 있다.
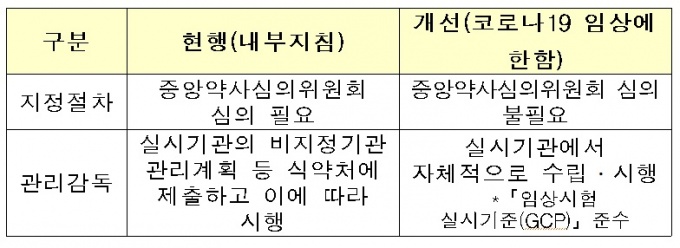
코로나19 환자를 대상으로 한 임상시험은 ‘실시기관’으로 지정되지 않았더라도 지정받은 기관의 관리‧감독 하에 참여할 수 있도록 허용한다.
신청자료 중 OECD 비(非)회원국에서 실시한 비임상시험 자료에 대해서 해외 실태조사를 서류평가로 대체한다.
또 의약품 등 제조(수입)관리자 및 안전관리책임자에 대한 교육 이수 의무기한을 올해 12월까지 일괄 연장한다.
소해면상뇌병증(Bovine Spongiform Encephalopathy, BSE) 미감염 증명서 제출 대상 의약품은 ’책임자가 전자 서명한 자료’를 우선 제출하고, 일정 유예기간 후 원본을 제출토록 허용했다.
식약처는 "코로나19 치료제‧백신 개발 지원 등 직접적인 위기 극복 방안을 추진함과 동시에 의약품 안전은 확보하면서도 제약업계 부담을 완화할 수 있도록 적극행정을 지속적으로 발굴, 추진하겠다"고 밝혔다.
 코로나19 환자를 대상으로 한 임상시험은 ‘실시기관’으로 지정되지 않았더라도 지정받은 기관의 관리‧감독 하에 참여할 수 있도록 허용한다.
코로나19 환자를 대상으로 한 임상시험은 ‘실시기관’으로 지정되지 않았더라도 지정받은 기관의 관리‧감독 하에 참여할 수 있도록 허용한다.