
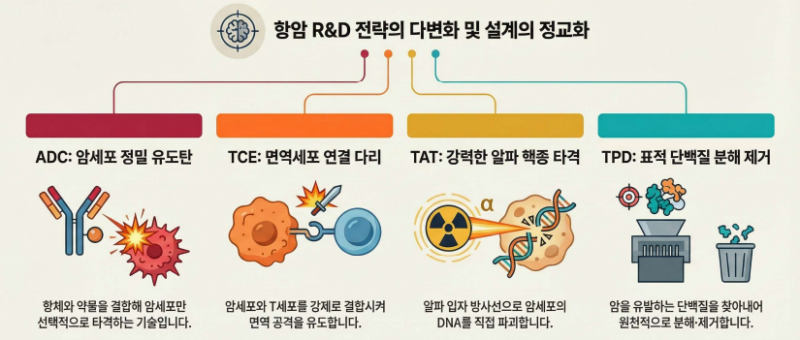
기존 ADC(항체-약물접합체) 중심에서 TCE(T세포 인게이저), TAT(표적 알파 치료), TPD(표적 단백질 분해) 등 차세대 모달리티가 잇따라 임상에 진입하고 있다.
14일 한국바이오의약품협회(KoBIA)가 2024년~2026년 1분기 FDA IND 승인 사례 중심으로 취합한 ‘최신 항암 R&D 전략 동향’ 보고서에 따르면 차세대 항암제가 ADC를 비롯해 TCE, TAT, TPD 등으로 다변화하고 있다.
보고서는 최근 항암 연구가 기존 접근을 반복하기보다 신규 표적 발굴과 작동기전, 전달기술 다변화로 치료 선택지를 넓히는 방향으로 재편되고 있다고 분석했다.
종양 이질성과 내성, 독성 문제로 인해 하나의 작동기전만으로는 다양한 환자군을 포괄하기 어렵다는 한계가 분명해지면서 신규 표적 발굴과 전달기술 고도화 등 치료 선택지를 넓히고 있다.
글로벌 항암제 시장이 2025년 약 2500억달러에서 연평균 11.5% 성장해 2034년 약 6680억달러 규모에 이를 것이란 전망이 나온다. 의료적 수요와 기술 혁신이 맞물리면서 핵심 성장영역으로 부상하고 있다는 분석이다.
최근 FDA로부터 IND 승인을 받은 주요 후보물질들은 각기 다른 혁신 기술을 탑재하고 있다.
ADC 분야에서는 애드센트릭스 ADRX-0405가 전립선암 등 고형암에서 과발현되는 신규 표적 STEAP1을 겨냥해 승인 받았다. 아이디야 바이오사이언스 IDE034는 B7H3와 PTK7 두 표적이 동시 발현될 때만 작동하도록 설계돼 선택성을 높였다.
TCE에서는 온코C4의 AI-081이 PD-1과 VEGF를 동시에 타격하는 이중특이항체로 2024년 승인을 획득했다. A2 바이오테라퓨틱스의 A2B543은 고형암 치료를 위한 CAR-T 후보물질로 2026년 1월 패스트트랙 지정을 동반해 승인됐다.
차세대 방사선 치료인 TAT 분야는 국내 기업인 SK바이오팜의 SKL35501가 NTSR1 발현 고형암을 대상으로 2025년 1월 FDA IND 승인을 마쳤다.
단백질 분해 기술인 TPD 분야에서는 시드 테라퓨틱스의 ST-01156이 유잉육종 등 난치성 고형암을 대상으로 2025년 8월 승인을 받았다.
2026년에는 주요 암 학회를 통해 이 같은 R&D 성과들이 대거 공개될 예정이다.
한국바이오의약품협회 측은 “기존 면역항암치료가 제한되는 경우를 대비해 면역세포를 직접 암세포에 붙여 공격하거나 면역반응을 보강하는 방식 등 대안이 개발되는 추세”라며 “유망 기술을 선별해 공동개발 투자 등 전략적 의사결정이 빠르게 진행될 것”이라고 전망했다.

ADC(-) TCE(T ), TAT( ), TPD( ) .
14 (KoBIA) 2024~2026 1 FDA IND R&D ADC TCE, TAT, TPD .
, .
, .
2025 2500 11.5% 2034 6680 . .
FDA IND .
ADC ADRX-0405 STEAP1 . IDE034 B7H3 PTK7 .
TCE C4 AI-081 PD-1 VEGF 2024 . A2 A2B543 CAR-T 2026 1 .
TAT SK SKL35501 NTSR1 2025 1 FDA IND .
TPD ST-01156 2025 8 .
2026 R&D .
“ ” “ ” .

