
 한국MSD 면역항암제 ‘키트루다’가 위암 분야 급여 확대 첫 관문인 약제급여평가위원회를 통과했다. 경쟁 약물인 오노약품공업 ‘옵디보’ 역시 같은 적응증으로 나란히 급여 적정성을 인정받았다.
한국MSD 면역항암제 ‘키트루다’가 위암 분야 급여 확대 첫 관문인 약제급여평가위원회를 통과했다. 경쟁 약물인 오노약품공업 ‘옵디보’ 역시 같은 적응증으로 나란히 급여 적정성을 인정받았다.
건강보험심사평가원은 지난 3월 5일 ‘2026년 제3차 약제급여평가위원회’를 열고 심의 결과를 공개했다.
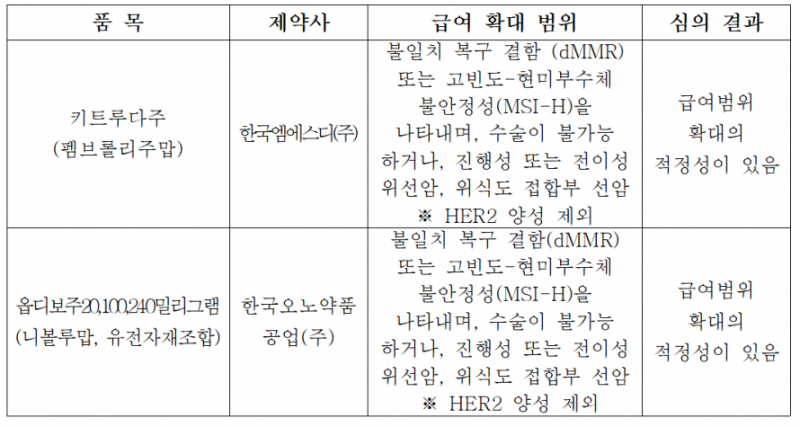
이번 약평위 논의 핵심은 면역항암제의 위암 급여 확대 여부였다. 심의 결과, 한국MSD의 키트루다주(펨브롤리주맙)는 ‘불일치 복구 결함(dMMR) 또는 고빈도-현미부수체 불안정성(MSI-H)을 나타내며 수술이 불가능하거나 진행성 또는 전이성인 위선암, 위식도 접합부 선암(HER2 양성 제외)’에 대해 급여 확대 적정성이 있는 것으로 심의됐다.
이번 결정으로 키트루다는 기존 급여 범위 외에 위암 치료 영역에서도 건강보험 적용을 위한 발판을 마련하게 됐다.
키트루다와 함께 안건에 오른 한국오노약품공업 옵디보주(니볼루맙) 역시 동일한 적응증(dMMR 또는 MSI-H 위선암·위식도 접합부 선암)에 대해 급여범위 확대 적정성을 인정받았다. 두 대형 면역항암제가 나란히 위암 1차 치료 시장 진입을 예고하며 치열한 경쟁을 이어갈 전망이다.
 한편, 이날 회의에서는 신규 등재를 노리는 약제들에 대한 심의도 진행됐다.
한편, 이날 회의에서는 신규 등재를 노리는 약제들에 대한 심의도 진행됐다.
바이엘코리아 전립선암 치료제 뉴베카정300mg(다로루타마이드)은 ▲고위험 비전이성 거세저항성 전립선암(nmCRPC) ▲호르몬 반응성 전이성 전립선암(mHSPC) 환자 치료(도세탁셀 및 ADT 병용 등)에 대해 효능·효과를 인정받았다.
다만 약평위는 뉴베카정에 대해 ‘평가금액 이하 수용 시 급여 적정성이 있다’는 조건을 달았다. 제약사가 정부가 제시한 약가를 수용해야만 급여권 진입이 가능하다는 의미다.
이 밖에 종근당 등 7개사의 뇌전증 치료제 브리베타정50mg 등 29품목(브리바라세탐)과 유니메드제약의 안구건조증 치료 점안제 시스폴점안액(1회용) 역시 평가금액 이하 수용을 조건으로 급여 적정성을 인정받았다.
이번 약평위를 통과한 약제들은 향후 국민건강보험공단과의 약가 협상, 건강보험정책심의위원회(건정심) 의결을 거쳐 급여 적용 여부가 최종 확정된다.
? MSD ‘' . ’' .
MSD ‘' . ’' .
3 5 ‘2026 3 ’ .
. , MSD () ‘ (dMMR) - (MSI-H) , (HER2 )’ .
.
() (dMMR MSI-H ) . 1 .
 , .
, .
300mg() (nmCRPC) (mHSPC) ( ADT ) .
‘ ’ . .
7 50mg 29() (1) .
, () .

