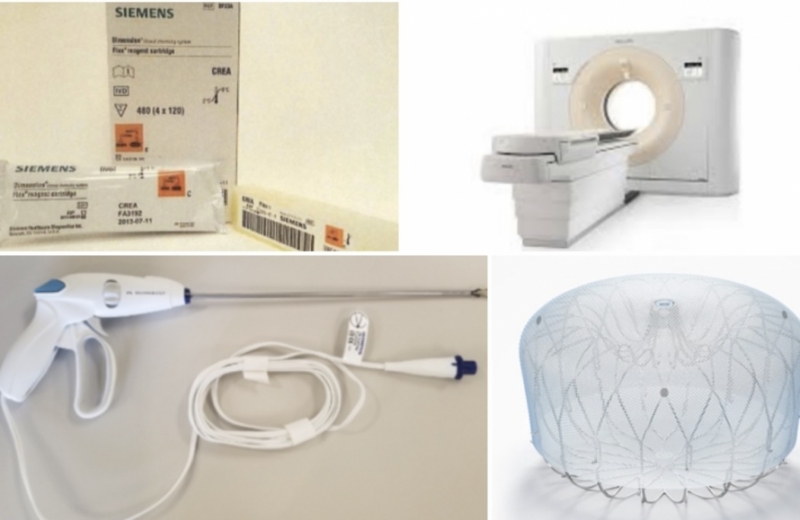
 지멘스헬시니어스, 필립스, 올림푸스한국, 보스톤사이언티픽코리아 등 글로벌 의료기기업체들이 일부 품목에 대한 영업자 회수 조치에 나섰다.
지멘스헬시니어스, 필립스, 올림푸스한국, 보스톤사이언티픽코리아 등 글로벌 의료기기업체들이 일부 품목에 대한 영업자 회수 조치에 나섰다.
의료기기통합정보시스템 정보에 따르면 지멘스헬시니어스는 '기타임상화학검사시약Ⅱ'에서 문제를 발견, 예방적 차원에서 회수 조치를 실시한다.
회사는 "Dimension 시스템(장비)에서 CRE2 시약 중 로트 GA6307 혹은 BA7005를 사용하는 경우 품질관리(QC) 및 환자 결과가 부정확할 가능성이 확인됐다"고 밝혔다.
이는 고객 불만 조사를 통해 확인한 사실로, 회사는 문제 예방을 위한 안내문 전달 및 교환 조치도 함께 진행 중이다.
필립스코리아는 전신용 전산화 단층 엑스선 촬영장치 소프트웨어에서 문제가 발생, 소프트웨어 업데이트 등 영업자 회수 조치에 들어갔다.
구체적으로 Philips IQon, iCT, Ingenuity, and Brilliance CT 64시스템에 영향을 미치는 다양한 소프트웨어 문제를 확인했다.
회사는 “내부 서비스팀(FSE)을 통해 해당 기기를 사용하는 고객사를 대상으로 소프트웨어 업데이트 설치토록 하고 있다”고 전했다.
미검증 구성품·미승인 부분품 포함 제품도 확인
올림푸스한국의 경우 일회용발조절식전기수술기용전극(모델명 920005PK, 3005,3005PK)과 일회용손조절식전기수술기용전극(PK-CF0533)에 대한 현장 시정 조치에 나선다.
해당 제품들은 호환되는 전기수술기와 연결해 내시경 수술, 복강경 및 개복 수술 시 조직 절개, 응고 및 조직을 잡아주는데 사용한다.
그러나 현장 시정 조치 대상 제품에선 공급업체가 용접공정을 적절히 검증하지 않은 구성품이 포함된 것으로 나타났다.
올림푸스한국은 "용접 불량은 사용 중 커팅 포셉(Cutting Forceps) 선단부가 파손되는 원인이 될 수 있다“며 ”회수 대상 수량이 방대해 회수기간을 3개월로 설정했다"고 전했다.
아울러 보스톤사이언티픽코리아는 아직 승인되지 않은 부분품(Hemostasis Valve)이 포함된 색전방어용기구가 수입된 사실을 확인해 해당 품목에 대한 자발적인 영업자 회수를 진행 중이다.
회사는 “이번 사안과 관련해 환자 안전에 대한 영향은 없다”며 “고객 불만 혹은 이상사례도 없었다”고 밝혔다.
그러면서 "해당 제품이 출고된 의료기관에 해당 사실을 알리고 미사용 제품은 즉시 사용중지 요청 후 회수 조치 진행하고 있다"고 알렸다.
 , , , .
, , , .
'' , .
"Dimension () CRE2 GA6307 BA7005 (QC) " .
, .
, .
Philips IQon, iCT, Ingenuity, and Brilliance CT 64 .
“ (FSE) ” .
( 920005PK, 3005,3005PK) (PK-CF0533) .
, , .
.
" (Cutting Forceps) “ ” 3 " .
(Hemostasis Valve) .
“ ” “ ” .
" " .
1년이 경과된 기사는 회원만 보실수 있습니다.

 지멘스헬시니어스, 필립스, 올림푸스한국, 보스톤사이언티픽코리아 등 글로벌 의료기기업체들이 일부 품목에 대한 영업자 회수 조치에 나섰다.
지멘스헬시니어스, 필립스, 올림푸스한국, 보스톤사이언티픽코리아 등 글로벌 의료기기업체들이 일부 품목에 대한 영업자 회수 조치에 나섰다.  , , , .
, , , . 
