

삼천당제약이 2500억 원 규모 블록딜 철회를 계기로 시장 진화에 나섰지만 미국 공급계약의 실체와 경구용 세마글루타이드 제네릭 여부, FDA 절차 해석 등을 둘러싼 핵심 쟁점에 대해서는 여전히 불확실성이 해소되지 않았다는 지적이 나온다.
삼천당제약(대표 전인석)은 6일 서울 삼천당제약 본사에서 기자간담회를 열고 메인 프로젝트 추진 현황과 경영 청사진 등을 공개했다.
삼천당제약은 지난달 24일 전인석 대표의 2500억 원 규모 블록딜 계획을 발표하며 시장에서 논란에 휩싸였다.
단기간 주가 상승 국면에서 대주주가 대규모 지분 매각에 나선 점을 두고 ‘고점 매각’ 논란이 불거진 데다, 회사가 강조해온 미국 공급 계약의 실체와 규모를 둘러싼 의구심까지 겹치며 투자자 불신이 확대됐다.
이날 전인석 대표는 “대주주로서 세금 납부를 위한 행위였지만 시장에서 악의적 해석이 확산되면서 기업 가치 훼손 우려가 커졌다”며 블록딜 철회 의사를 밝혔다.
이어 “사기극이라는 프레임에 굴복하지 않겠다”며 “차라리 이자 부담을 감수하고 추가 주식담보대출을 받겠다”고 말했다.
그는 자신과 배우자가 부담해야 할 세금이 약 2335억 원에 달한다고 공개했다. 구체적으로 지난해 증여 이후 1차로 약 390억 원을 주식담보대출로 조달해 납부했고, 이후 남은 증여세와 향후 지분 매각 시 발생할 양도소득세 등을 포함하면 총 세금 부담이 2000억 원을 상회하는 구조라는 설명이다.
또 블록딜 규모를 2500억 원으로 설정한 배경에 대해 “세금 외에도 주가 변동성에 대비한 안전장치 성격이 있었으며, 잔액 발생 시 재매입에 활용할 계획이었다”고 덧붙였다.
계약 구조 강조했지만…핵심 수치는 끝내 빠져
전 대표는 미국 계약 과장 논란에 대해 부인하며 “삼천당제약이 기술수출이 아닌 제품 공급 기반 계약 구조를 갖고 있다”고 강조했다.
그는 또 “파트너사가 매출 목표를 제시하고 이를 달성하지 못할 경우 계약 해지가 가능한 바인딩 조항이 포함돼 있다”고 설명했다.
하지만 목표 매출 규모와 해지 기준 금액 등 핵심 수치는 공개되지 않았다.
회사는 “공시 규정상 미래 매출을 기재할 수 없다”고 설명했지만, 투자 판단에 필요한 핵심 정보가 빠진 상태라는 지적이 나온다.
ANDA vs Pre-ANDA…경구용 세마글루타이드 ‘제네릭 논쟁’ 속 핵심 질문 회피
경구용 세마글루타이드의 제네릭 여부도 핵심 쟁점으로 떠올랐다. 최근 iM증권 애널리스트가 경구용 세마글루타이드의 추가 임상 필요성을 제기하자 회사는 해당 애널리스트를 고소하겠다고 밝히며 강경 대응에 나섰다.
삼천당제약은 그동안 해당 제품이 대규모 임상시험이 아닌 제네릭 개발 절차를 적용할 수 있다는 점을 지속적으로 강조해왔다. 즉, 수천억 원이 소요되는 임상시험이 아니라 상대적으로 입증 부담이 낮은 생물학적동등성 시험만으로 허가가 가능하다는 논리다.
이날 전 대표는 “FDA가 제네릭으로 분류해 ANDA 번호가 부여됐다”는 취지로 설명하면서 “추가 임상이 아닌 생물학적동등성 시험만으로 가능하다”고 주장했다.
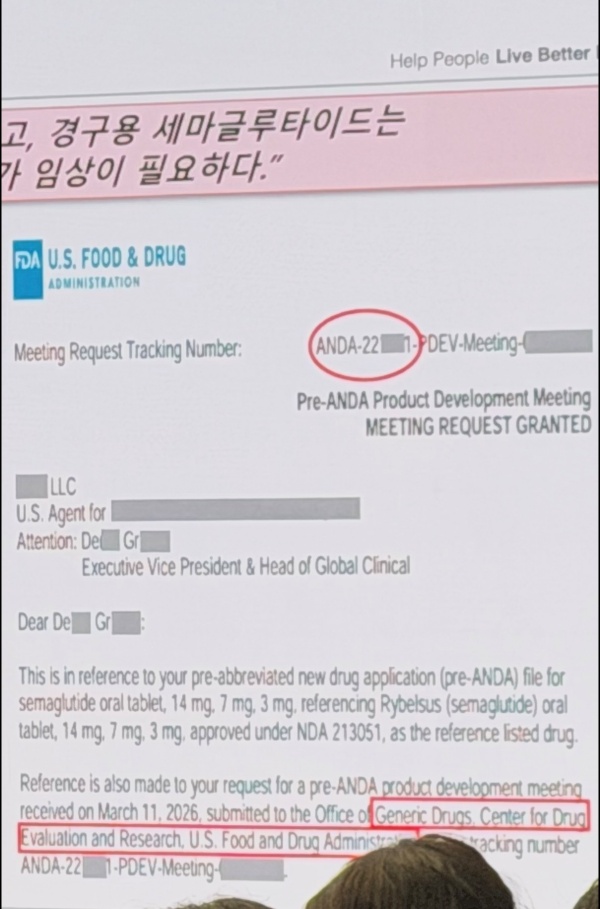 또 회사는 근거로 FDA 관련 문서를 공개했다.
또 회사는 근거로 FDA 관련 문서를 공개했다.
다만, 공개된 자료에는 “Pre-ANDA Product Development Meeting – MEETING REQUEST GRANTED(허가 전 사전협의 단계 제품 개발 관련 미팅 요청이 FDA에 의해 승인됨)”라는 문구와 함께 “pre-abbreviated new drug application (pre-ANDA)”라는 표현이 명시돼 있었다.
ANDA는 제네릭 의약품 허가를 위한 정식 신청 단계이며, Pre-ANDA는 그 이전 FDA와 개발·허가 요건을 사전 협의하는 단계다.
즉, FDA가 사전 미팅 요청을 승인했다는 내용으로 정식 ANDA 신청이 아닌 Pre-ANDA 단계임을 보여주는 자료다.
하지만 이후 질의응답에서는 혼선이 이어졌다.
기자들이 “제네릭이 가능한지 확인하는 사전 상담 단계가 아니냐. FDA가 생물학적동등성 시험만 해도 되는지 확답을 줬냐”고 수차례 질문했지만, 전 대표는 “미국 USP 가이드라인에 나와 있고 나중에 찾아오면 서류를 보여줄 수 있다”며 “최종 승인을 받은 건 아니지만 확답을 받았다고 볼 수 있다”고 답했다.
업계에서는 FDA 미팅 승인이나 서류 접수는 초기 절차일 뿐이며, 제네릭 인정이나 허가 가능성을 의미하지 않는다는 점에서 과도한 해석이라는 지적이 나온다.
특히 경구형 GLP-1 제제는 제형 특성상 추가 임상 요구 가능성이 지속적으로 제기돼온 분야라는 측면에서 논란이 이어지고 있다.
설명 이어졌지만…실무진 대응에 더 커진 의문
간담회 후반부에서는 일부 기술·계약 관련 세부 질문이 이어지자 전 대표가 “제가 설명이 매끄럽지 못한 부분이 있어 본부장이 설명을 해주겠다”고 말했고, 본부장이 보충 설명에 나섰다.
다만 해당 인물은 이름을 묻는 말에 답하지 않은 채 답변을 이어갔고, 끝내 현장을 벗어나면서 책임 있는 설명을 회피한 것 아니냐는 지적이 제기됐다.
이번 간담회는 주요 의혹에 대한 해명 성격이었지만 핵심 정보는 여전히 제한적으로만 공개됐다.
삼천당제약이 주장하는 기술과 계약 가치가 시장 신뢰를 회복하기 위해서는 보다 구체적이고 검증 가능한 정보 공개가 필요하다는 지적이 나온다.
전인석 대표는 “거짓을 말하거나 계약을 부풀린 적이 없다. 결국 결과로 증명할 수밖에 없다. 앞으로 오직 경영과 성과로 삼천당제약의 가치를 입증하겠다”고 강조했다.

2500 , FDA .
( ) 6 .
24 2500 .
‘ ’ , .
“ ” .
“ ” “ ” .
2335 . 1 390 , 2000 .
2500 “ , ” .
“ ” .
“ ” .
.
“ ” , .
ANDA vs Pre-ANDA ‘ ’
. iM .
. , .
“FDA ANDA ” “ ” .
 FDA .
FDA .
, “Pre-ANDA Product Development Meeting MEETING REQUEST GRANTED( FDA )” “pre-abbreviated new drug application (pre-ANDA)” .
ANDA , Pre-ANDA FDA .
, FDA ANDA Pre-ANDA .
.
“ . FDA ” , “ USP ” “ ” .
FDA , .
GLP-1 .
“ ” , .
, .
.
.
“ . . ” .?

