
 국내 최대 진단키트 업체인 에스디바이오센서 주력 제품이 실제 임상 현장에서는 정확도가 크게 떨어진다는 연구 결과가 나와 파장이 예상된다.
국내 최대 진단키트 업체인 에스디바이오센서 주력 제품이 실제 임상 현장에서는 정확도가 크게 떨어진다는 연구 결과가 나와 파장이 예상된다.
연구진은 이 같은 문제가 코로나19 확진자가 10만 명을 넘어서는 등 폭발적으로 증가한 배경에도 영향을 미쳤을 것으로 추정했다.
중앙대학교 의과대학 진단검사의학교실 임용관 교수팀은 최근 대한의학회 국제학술지 'Journal of korean medical science'에 코로나19 신속항원검사키트(RDT) 정확도에 대한 리얼월드데이터 연구 결과를 공개했다.
리얼월드데이터(Real World Data, RWD)란 임상시험이 끝난 시약을 실제 의료현장에서 사용하면서 수집한 데이터를 말한다. 일종의 4상격인 결과를 말한다.
연구팀은 코로나19 발발 이후 바이러스 감염 여부를 판단하기 위해 무수한 RDT가 사용됐지만, 정확도에 대한 연구는 진행되지 않았다는 이유에서 실험을 추진했다.
연구팀은 업계 대표격인 에스디바이오센서 'STANDARD Q COVID-19 Ag(STANDARD Q)'을 시험 대상에 올렸다.
실험은 2020년 12월부터 2022년 4월까지 RDT와 RT-PCR(역전사중합효소연쇄반응)을 동시에 받은 5792명을 대상으로 진행됐다. 각각 주기 임계값인 CT값을 동일하게 설정하고 검출 한계(LOD)를 추정하기 위해 이항 로지스틱 회귀분석을 진행해 비교한 것이다.
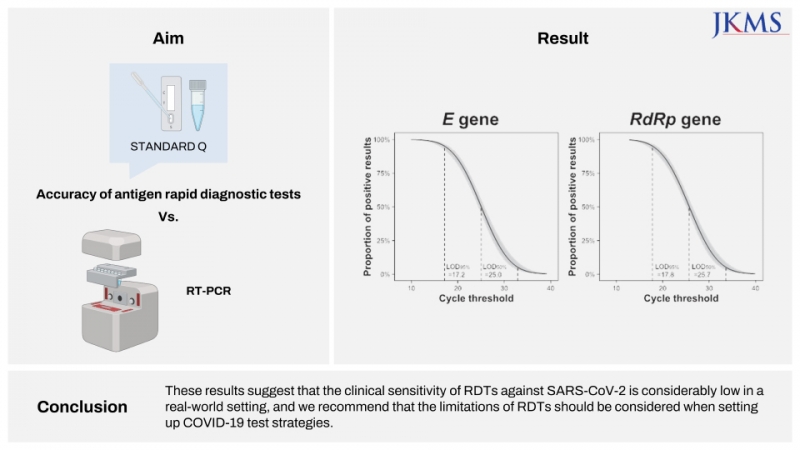
그 결과, RDT와 RT-PCR을 모두 시행한 환자 중 418명이 확진된 것으로 파악됐다. 또 36명이 불확정 판정을 받았으며 5042명이 음성으로 판명됐다.
주목할 점은 RT-PCR에서 양성이 나온 환자 418명 중 RDT에서 양성이 나온 환자는 239명에 불과하다는 것이다. 이는 STANDARD Q 민감도가 57.2%에 불과하다는 의미다.
세계보건기구(WHO) 지침에 따르면 RDT는 민감도 80% 이상, 특이도 97% 이상을 최소 요구 사항으로 제시하고 있다.
하지만 STANDARD Q의 경우 WHO 기준에 한참 미치지 못하고 있다는 게 연구팀 주장이다. 실제로 에스디바이오센서는 STANDARD Q가 민감도 90%, 특이도 96%를 기록했다고 명시하고 있다.
연구팀은 "결국 확진자 검사에 RDT를 사용했을때 수많은 양성 환자가 음성으로 분류됐다는 의미"라면서 "코로나19 확진자가 급증한 배경에도 이러한 문제가 영향을 미쳤을 것으로 추정한다"고 설명했다.
이에 대해 에스디바이오센서 측은 해당 연구 결과를 받아들일 수 없다는 입장이다.
에스디바이오센서 관계자는 "연구진 활동에 대해서는 존중하지만 실험 프로토콜에 대한 기준이 명확하지 않다"면서 "회사는 WHO 지침에 따라 요구 사항을 준수하고 있다"고 설명했다.
이와 관련, 임용관 교수는 "제품설명서에 명시된 민감도와 특이도 평가에 사용된 검체 상세정보가 제공되지 않으면, 키트 성능에 대한 정보를 받아들이기 어렵다"며 "제품을 개발하면서 사용한 시험 프로토콜 신뢰도부터 확인해야 한다"고 말했다.
그러면서 "검사를 받는 피검사자가 RDT 한계점을 전달받을 수 있도록 하고, 일반인을 대상으로 하는 광고에서도 유명 연예인을 기용한 감성마케팅으로 키트 장점만을 부각하는 홍보는 지양해야 한다"고 강조했다.
