
 지난해 국내에서 임상시험 승인을 가장 많이 받은 기관은 '삼성서울병원'이었다. 제약사별로는 노바티스(외자사)와 한미약품(국내사)이 꼽혔다.
지난해 국내에서 임상시험 승인을 가장 많이 받은 기관은 '삼성서울병원'이었다. 제약사별로는 노바티스(외자사)와 한미약품(국내사)이 꼽혔다.
22일 식품의약품안전처가 발표한 '2017년 임상시험계획 승인 현황 분석 결과'에 따르면 전체 승인건수는 658건으로 2016년 628건 대비 4.8% 증가했다.
구체적으로 보면, 전체 임상시험 승인 658건 가운데 연구자임상(의료기관)이 182건(27.7%), 제약사 임상이 476건(72.3%)을 차지한다. 이 중 다국적 제약사는 293건(44.5%), 국내사 183건(27.8%)를 차지한다.
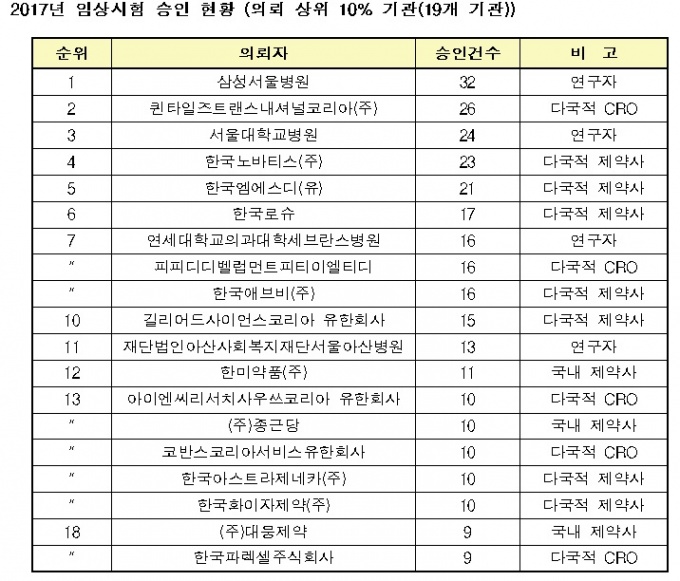
이중 임상 승인 기관 상위 10%로 19개 기관이 집계됐다. 눈에 띄는 점은 '빅4' 병원이 여기에 모두 포함됐다는 것이다.
지난해 임상시험 승인을 가장 많이 획득한 기관은 삼성서울병원으로 32건을 기록, 전체 1위를 차지했다. 이어 서울대병원은 24건, 연세세브란스병원 16건, 서울아산병원 13건으로 각각 3위, 7위, 11위에 올랐다.
연구자(의료기관) 임상은 꾸준히 증가하는 추세다. 2015년 134건(19.9%)에서 2016년 171건(27.2%), 2017년 182건(27.7%)로 매년 늘고 있다.
물론, 임상 승인 규모만 보면 제약사가 월등히 높은 비중을 차지한다. 2015년 540건(80.1%), 2016년 457건(72.8%), 2017년 476건(72.3%)으로 건수는 많지만, 비율은 하락하는 추세다.
제약사별로 보면 다국적 제약사 가운데 한국노바티스가 23건, 한국엠에스디 21건, 한국로슈 17건 순으로 나타났다.
국내사의 경우 한미약품이 11건으로 가장 많았고, 종근당 10건, 대웅제약 9건 등이 뒤를 이었다.
식약처 관계자는 "국내 임상시험은 전 세계 임상시험 감소 추세 속에서도 임상시험 수행을 위한 제도와 시설‧인력 등 인프라가 다른 국가에 비해 경쟁력을 갖추고 있어 늘어나고 있다"고 말했다.
또 하나 주목해야 할 포인트는 전체 임상에서 면역항암제 승인과 다국가 3상 승인이 30% 이상 급증했다는 점이다.
지난해 실시된 임상시험을 효능군별로 살펴보면 항암제(251건), 심혈관계(61건), 중추신경계(54건), 내분비계(45건), 소화기계(41건) 등의 순으로 나타났다.
승인 건수가 가장 많은 항암제는 작용기전별로 표적항암제가 114건(45.4%)으로 가장 많았고 면역항암제(89건, 35.5%)가 뒤를 이었다.
표적항암제는 특정 표적인자만 선택적으로 공격하는 항암제로 2015년 123건, 2016년 86건, 2017년 114건이 승인됐다.
면역항암제는 2016년 68건 대비 30.9%나 늘어난 89건으로 나타났다. 기존 화학항암제에 비해 부작용이 적고 다양한 암에 사용할 수 있는 장점으로 개발이 활발히 이뤄지고 있다.
치매치료제 개발에 대한 관심이 높아지고 있는 가운데 치매치료제 임상시험 승인은 17건으로 전년(16건)과 비슷했으나 5건은 초기(1상) 시험으로 치매 치료제 개발을 위한 초기 개발·연구가 활발히 이뤄지고 있는 것으로 풀이된다.
제약사 임상시험 중에서는 국내외에서 실시하는 다국가 임상이 293건 승인돼 9.7% 증가했다. 다국가 임상시험 중에서도 품목허가 전 마지막 단계인 3상 승인이 2016년 136건에서 지난해 178건으로 30.9% 뛰었다.
식약처 관계자는 "최근에는 암세포를 죽이거나 성장을 억제하는 항암치료에서 면역세포를 활성화시켜 암을 치료하는 면역항암 치료로 전환되는 추세가 국내 임상시험에도 반영되고 있는 것으로 보인다"고 설명했다.
