[데일리메디 양보혜 기자] 대웅제약이 국내 최초로 개발 중인 SGLT-2 억제제 계열 당뇨 신약 ‘이나보글리플로진’이 주요 적응증을 동시에 획득하기 위한 임상 3상을 승인 받아 개발이 가속화될 전망이다.
대웅제약(대표 전승호)은 지난 9월29일 식품의약품안전처로부터 ‘이나보글리플로진’의 단독요법, 메트포르민 병용요법 각각에 대한 유효성과 안전성을 평가하는 3상 임상시험을 동시에 승인 받았다고 6일 밝혔다.
단독 사용 임상시험은 제2형 당뇨병 환자 140여 명을 대상으로 서울대병원 등 전국 30여 대형병원에서 진행된다.
또한 메트포르민으로 혈당 조절이 불충분한 제 2형 당뇨병 환자 190여명 대상의 메트포르민 병용 사용 임상시험은 가톨릭대 서울성모병원을 포함 전국 30여개 대형병원에서 진행될 예정이다.
'이나보글리플로진'은 콩팥에서 포도당의 재흡수에 관여하는 SGLT-2수용체를 선택적으로 억제함으로써, 포도당을 직접 소변으로 배출시키는 기전을 가졌다.
 대웅제약은 지난 9월 국제학술대회 '2020 ICDM'에서 성공적인 임상 2상 결과를 최초 공개한 바 있다.
대웅제약은 지난 9월 국제학술대회 '2020 ICDM'에서 성공적인 임상 2상 결과를 최초 공개한 바 있다.
그 결과, 혈당 조절 주요지표인 당화혈색소(HbA1c)의 12주 후 변화량이 위약 대비 약 0.9%로, 이는 서양인들을 대상으로 진행됐던 기존 SGLT-2억제제보다 30%가 넘는 효과적인 감소를 보였다.
대웅제약 관계자는 "국제적인 당뇨병 조절 목표인 ‘당화혈색소 7.0% 이하로 도달한 환자 비율’이 최대 61%에 달해 기존 SGLT-2 억제제보다 20% 이상 좋은 결과를 나타냈다"고 밝혔다.
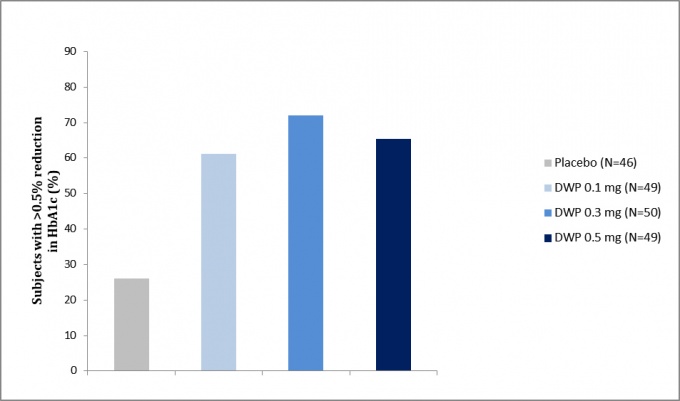
그는 "치료 전(前) 대비 당화혈색소 0.5% 초과 감소한 환자비율은 동일 계열 약물의 40~60% 수준 대비 최대 72%를 기록해 탁월한 혈당감소 효과를 추가로 입증했다"고 덧붙였다.
