의사
의사
채용
코로나19 초간단 진단시약 추가 승인
식약처, 9개 제품 허가…1시간 이내 신속검사 체계 구축
[데일리메디 한해진 기자] 식품의약품안전처(처장 이의경)는 질병관리본부의 코로나19 진단시약 긴급사용 승인 요청에 대해 적합한 9개 제품을 승인했다고 24일 밝혔다.
이는 질병관리본부가 응급용 선별검사 진단시약의 긴급사용 신청 공고를 통해 접수한 13개 제품을 검토한 최종 결과다.
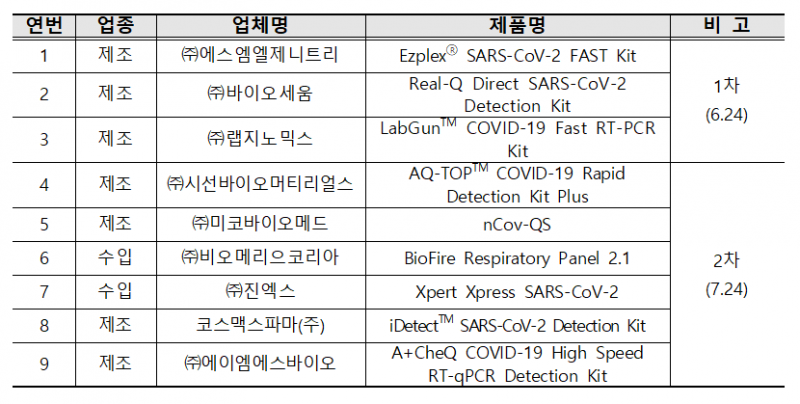
6월 24일에는 에스엠엘제니트리·바이오세움·랩지노믹스의 진단시약이 허가를 받았고 7월 24일 기준으로 시선바이오머티리얼스·미코바이오메드·비오메리으코리아·진엑스·코스맥스파마·에이엠에스바이오 등이 허가됐다.
특히 이들 제품은 검체 전처리부터 결과 도출까지 1시간 이내에 가능한 조건을 갖췄다.
식약처 관계자는 "의료기관에서 실시한 임상적 성능시험 및 제품 성능과 의료현장 사용 적합성 등에 대해 전문가 심의를 거쳐 종합적으로 평가한 후, 긴급사용 제품으로 최종 승인했다"고 설명했다.
이번 긴급사용승인 제품은 응급환자의 처치가 지연되는 것을 방지하는 등 신속검사 체계를 구축하는데 도움이 될 것으로 보인다.
식약처는 코로나19에 대한 방역 대응을 위해 승인받은 진단시약 생산·수급 상황을 모니터링해 안정적인 수급을 유지할 수 있도록 업체와 긴밀히 협조해 나간다는 방침이다.