
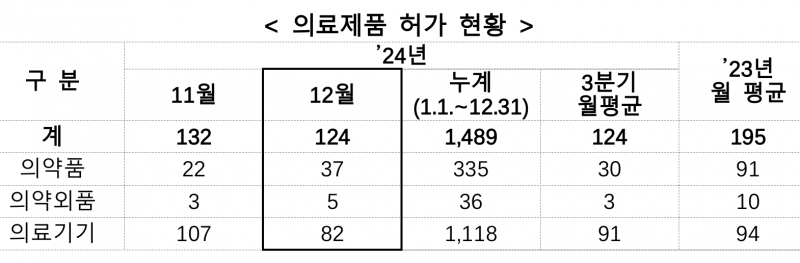
 작년 한해 국내에서 허가된 의약품은 총 335개이며 의료기기는 1118개로 확인됐다.
작년 한해 국내에서 허가된 의약품은 총 335개이며 의료기기는 1118개로 확인됐다.
식품의약품안전처(처장 오유경)는 이 같은 내용을 담은 지난해 12월 의료제품 허가 현황을 9일 공개했다.
구체적으로 보면 2024년 1월 1일부터 12월 31일까지 식약처는 의료제품 총 1489개를 품목허가했다. 이중 의약품은 335개, 의료기기는 1118개, 의약외품은 36개다.
12월 한달 간을 기준으로 보면 의약품 37개, 의료기기 82개, 의약외품 5개가 허가됐다. 2023년 월평균(195개) 대비 63.6%로 감소했지만, 2024년 3분기 월평균(124개)과 같은 수준이었다.
식약처는 비마약성 진통제 ‘어나프라주(오피란제린)’, 호흡기세포융합바이러스(RSV)에 의한 하기도 질환 예방 백신 ‘아렉스비주(유전자재조합)’를 신약으로 허가했다.
또한 소아 연골무형성증 치료제 ‘복스조고주0.4mg·0.56mg·1.2mg(보소리타이드)’과 간질성폐질환 치료제 ‘닌테브로정100mg·150mg(닌테다닙에실산염)’을 희귀의약품으로 허가했다.
아울러 의료기기에서는 인공지능(AI) 기반으로 환자 면담기록 데이터를 분석한 후 우울증 확률을 수치화해 표시, 의사들의 우울증 진단을 보조할 수 있는 국내 첫 번째 소프트웨어(심리평가소프트웨어) ‘ACRYL-D01’을 허가했다.
식약처는 “앞으로도 안전하고 유효한 제품을 신속히 허가해 환자 치료 기회를 지속 확대해 나가는 동시에 의료제품 허가 현황을 정기적으로 제공하는 등 의료제품 허가심사에 대한 투명성과 신뢰성도 강화해 나갈 계획”이라고 전했다.
한편, 이번 품목허가 집계에는 지방식품의약품안전청 허가품목은 제외한 본부 허가 품목만 포함됐다.
 ? 335 1118 .
? 335 1118 .
( ) 12 9 .
2024 1 1 12 31 1489 . 335, 1118, 36.
12 37, 82, 5 . 2023 (195) 63.6% , 2024 3 (124) .
(), (RSV) () .
0.4mg0.56mg1.2mg() 100mg150mg() .
(AI) , () ACRYL-D01 .
“ ” .
, .

