
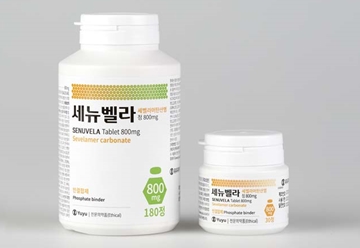
 만성신장병 환자의 고인산혈증을 치료하는 세벨라머탄산염 성분 제네릭 시장 경쟁이 가열되고 있는 가운데 처음으로 저용량 제품이 등장했다.
만성신장병 환자의 고인산혈증을 치료하는 세벨라머탄산염 성분 제네릭 시장 경쟁이 가열되고 있는 가운데 처음으로 저용량 제품이 등장했다.
식품의약품안전처는 지난 10일 유유제약 ‘세뉴벨라정400mg’(성분명 세벨라머탄산염)을 허가했다.
오리지널 의약품인 사노피-아벤티스 ‘렌벨라정’도 보유하지 않은 용량이다.
해당 품목은 △투석을 받고 있는 만성 신장질환자 혈청 인 조절 △투석을 받고 있지 않은 만성 신장질환자 중 혈청 인 농도가 5.5 mg/dl 이상인 환자 혈청 인 조절 등에 쓰인다.
유유제약은 지난 2022년 세뉴벨라정800mg에 대한 허가를 획득했다. 기존 고용량은 투석을 받고 있는 만성 신장질환자의 혈청 인 조절에 대한 적응증만 가졌다.
이에 반해 저용량 품목의 경우 고용량 적응증에 투석을 받고 있지 않은 만성 신장질환자 중 혈청 인 농도가 5.5 mg/dl 이상인 환자의 혈청 인 조절에도 사용할 수 있다.
고인산혈증 처방 시장은 지난 2011년 처음 허가된 사노피-아벤티스 ‘렌벨라정’과 2015년 허가된 SK케미칼 ‘인벨라정’이 양분하고 있었다.
렌벨라정의 경우 수입 완제의약품이고, 인벨라정은 스페인 제약사로부터 완제품를 받아 국내 제약사에서 공급하고 있어 수입 의존도가 높은 품목으로 꼽혔다.
하지만 국내 제약사들이 2022년부터 제네릭 허가를 받으면서 판도가 바뀌었다. 2022년 4월 대원제약의 ‘세머원정’이 허가 받은 후 같은 해 6월 유유제약이 ‘세뉴벨라정’에 대한 허가를 획득했다.
이후 보령 ‘인세벨정’, 알보젠코리아 ‘젠벨라정800mg’, 팜젠사이언스 ‘벨라비엠정’이 합류했고 여기에 대웅제약 ‘세벨머정’, 퍼슨 ‘레나벨정’도 참전하면서 허가 품목이 총 11개로 늘었다.
이런 가운데 유유제약은 기존에 보유한 품목의 용량을 절반 줄인 400mg을 약 2년 만에 선보이며 차별화에 나섰다.
업계 관계자는 "고인산혈증은 뼈를 구성하는 무기질 중 하나인 인이 정상치보다 높아 뼈가 약해져 골절이 쉽게 생기는 질환으로 주로 신부전 환자에게 많이 발병한다"고 설명했다.
이어 “이를 치료하기 위해 기존에는 칼슘 함유 인결합제를 많이 사용했으나 최근에는 세벨라머, 탄산란탄 제제 등의 등장으로 치료옵션이 늘어나는 추세”라고 덧붙였다.
 ? .
? .
10 ‘400mg’( ) .
- '' .
5.5 mg/dl .
2022 800mg . .
5.5 mg/dl .
2011 - ‘' 2015 SK ’' .
, .
2022 . 2022 4 ‘' 6 ’' .
‘', ’800mg‘, ’‘ ’‘, ’' 11 .
400mg 2 .
" " .
“ , ” . ???

