[데일리메디 신지호기자] 식품의약품안전처는18일 다국적제약 화이자가 코로나19 백신에 대한 허가신청 전(前) 비임상 및 임상 1·2·3상 자료에 대한 사전검토를 신청했다고 밝혔다.
의약품 품목 허가를 위한 자료를 제출한 것이다. 품목허가 승인 후 국가출하 승인 절차를 거치면 국내 유통이 가능해진다.
식약처 관계자는 "같은 날 아스트라제네카도 코로나19 백신 허가신청 전 품질자료에 대한 추가 사전검토를 신청했다"고 밝혔다.
제약사 모더나와 얀센의 코로나19 백신에 관한 자료는 아직 식약처에서 검토중이지 않은 것으로 파악됐다.
17일 식약처 관계자는 데일리메디와의 통화에서 "화이자, 아스트라제네카 임상 자료 검토 초기 단계이며 모더나, 얀센 자료는 없다”고 전했다.
미국과 영국은 화이자 백신 접종을 시작한 상황에서 한국은 이제 사전 검토 승인 신청이 들어간 이유는 정부와 화이자 협상이 늦게 시작됬기 때문인 것으로 보인다.
식약처 관계자는 "화이자 코로나19 백신 자료에 대한 식약처 검토는 화이자와의 협상과정 일환으로 정부와 공급 계약이 어느정도 확정 됐을 때 제약사 측에서 자료를 넘긴다"고 밝혔다.
그는 “화이자의 경우 ‘한국화이자’가 있기 때문에 공급라인에 문제가 없지만 모더나는 국내 공급라인이 없어 아직 확실한 계약이 이뤄지지 않았고 자료도 받은게 없다”고 덧붙였다.
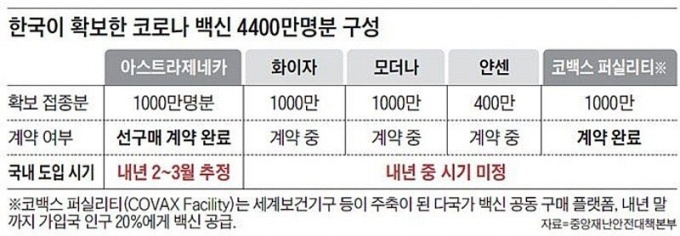
지난 8일 정부는 해외 제약사와 개별 계약을 통해 확보하려는 3400만명분, 총 6400만 도즈(1회 접종분) 계약 체결 진행 상황을 발표했다.
아스트라제네카와 화이자·모더나 각 2000만 도즈, 존슨앤드존슨-얀센 400만 도즈로 이 중 아스트라제네카와는 계약을 마쳤으며, 화이자, 존슨앤드존슨-얀센, 모더나와는 구매 확정서, 공급 확약서 등 법적 구속력이 있는 합의를 통해 구매 물량을 확정했다고 밝혔다.
정부는 18일에도 백신 계약 관련 내용을 발표했는데 제조사별 공급 수량에는 변함이 없고 계약 진행상황이 소개됐다.
얀센이 다음 주 계약이 완료될 것과 화이자 계약서도 최종 검토인 법률 검토를 하고 있는 단계다.
화이자, '품목허가' 이어 '국가출하승인' 거치는 등 접종까지는 다소 시간 걸릴 수 있어
정부가 외국 제약사로부터 구입한 백신은 특례수입(긴급사용승인)이 아닌 정식 품목 허가를 거쳐 들여오는 방식이다.
화이자 백신을 국민이 접종하기 까지 '품목허가'와 '국가출하승인' 제도를 거쳐야한다.
통상 품목허가 90일, 국가출하승인은 60일 총 5개월이 소요된다. 하지만 정부는 이 기간을 단축하겠다고 밝혔다.
의약품 품목 허가에 신속 심사를 진행해 허가에 걸리는 90일을 40일로 앞당기고 60일 걸리는 국가출하승인을 20일로 줄여 백신 승인을 최단 시간에 하겠다는 것이다.
승인이 끝이 아니다. '승인=공급시작'이 아니기 때문이다. 백신 물량이 확보되지 않으면 승인이 빨라도 문제가 된다.
가령 화이자 백신을 1월에 계약 공급을 맺고 구입을 해 그때부터 2개월에 걸쳐 3월에 승인한다하더라도 백신을 맞기까지 대기 시간이 필요하다. 국내에 화이자 백신 물량이 없을 수 있기 때문이다.
현재 화이자 백신의 경우 미국 등 주요국들이 제약사와 개별 구매를 통해 백신 물량을 싹쓸이해 품귀현상이 벌어지고 있다.