
 지난 3월 건강보험심사평가원 암질환심의위원회(이하 암질심)에서 재심의 대상으로 분류됐던 유방암 치료제 엔허투가 급여화에 바짝 다가섰다.
지난 3월 건강보험심사평가원 암질환심의위원회(이하 암질심)에서 재심의 대상으로 분류됐던 유방암 치료제 엔허투가 급여화에 바짝 다가섰다.
또 국내 판매 중단 사태를 겪었던 연조직 육종 희귀암 치료제 욘델리스도 암질심 문턱을 넘어 급여화 가능성을 높였다.
두 치료제 모두 항암제 급여 적용과 타당성을 검토하는 암질심을 통과함에 따라 약제급여평가위원회 심사와 약가협상 과정을 거쳐 건강보험정책심의위원회에서 급여적용 여부가 최종 결정된다.
심평원은 3일 암질심을 통해 진행된 ‘암환자에게 사용되는 약제에 대한 급여기준 심의결과’를 공개했다.
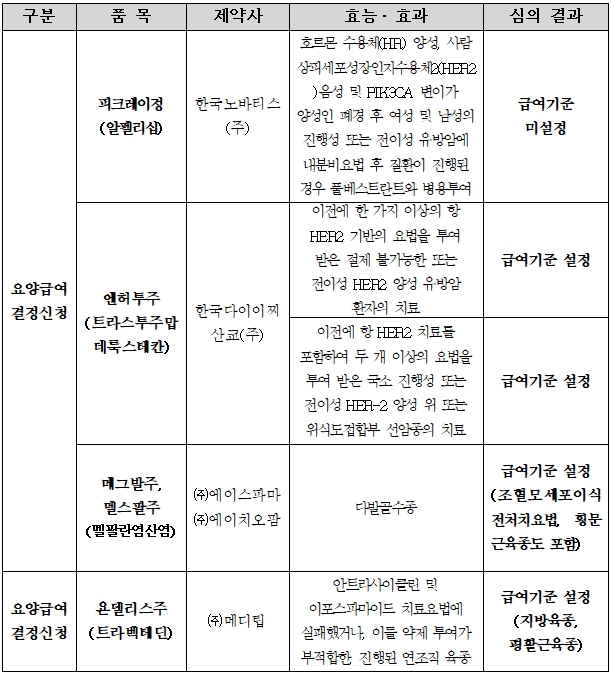
요양급여 결정신청에 따른 심의 결과, 한국다이이찌산쿄 엔허투와 메디팁 욘델리스가 급여 타당성 검토를 통과해 급여화를 위한 본격적인 과정에 돌입했다.
엔허투의 효능‧효과는 이전에 한 가지 이상의 항 HER2기반의 요법을 투여받은 절제 불가능한 또는 전이성 HER2 양성 유방함 환자 치료로 인정받았다.
또 이전에 항 HER2 치료를 포함해 두 개 이상의 요법을 투여 받은 국소 진행성 또는 전이성 HER-2 양성 위 또는 위식도접합부 선암종의 치료 활용도 허용됐다.
욘델리스는 안트라사이클린 및 이포스파마이드 치료요법에 실패했거나 이들 약제 투여가 부적합한 진행된 연조직 육종으로 효과가 설정됐다.
에이스파마와 에이치오팜의 메그발주와 멜스팔주도 다발골수종의 치료 효과를 인정받으며 급여기준 설정의 문턱을 넘었다. 급여기준에는 조혈모세포이식, 전처치요법, 횡문 근육종도 포함됐다.
반면 한국노바티스의 피크레이는 통과에 실패했으며, 급여기준 확대를 신청한 한국릴리의 버제니오와 한국로슈의 티쎈트릭도 심사 문턱을 넘지 못했다.
한국아스텔라제약의 조스파타와 한국얀센의 다잘렉스도 급여기준 확대의 문턱을 통과했다.
사회적 요구 컸던 엔허투·욘델리스, 환자 선택지 확대 기대
영국 등 해외에서도 엔허투의 보험이 인정된 상태며 심사통과 이후 처방이 크게 늘 것으로 전문가들은 내다보고 있다.
HER2 양성 유방암의 2차 표준 선택지로 주목받는 엔허투는 급여 적용 이후 모든 HER2 양성 환자에게 투약함은 물론 적응증 확대로 추가적인 사용 확대까지 예상되는 것이다.
앞서 엔허투는 국민청원을 통해 5만 명이 건강보험 급여 등재를 요구하는 등 사회적으로 주목받으며 급여 가능성이 높게 점쳐졌다.
또 국내 판매 중단됐던 욘델리스 역시 암질심 문턱을 넘으며 출시 15년 만에 급여권에 진입 가능성을 높이며 순항을 시작했다.
욘델리스의 적응증인 연조직(연부조직) 육종은 성인 악성종양의 1%를 차지하는 희귀 암으로 관련 신약 출시가 없음에도 급여화가 장기간 이뤄지지 않아 환자들의 불만이 높았다.
앞서 2021년 6월 욘델리스의 공급 중단이 결정됐으며, 완전동일 성분의 대체약제는 없지만 연조직 육종에 사용되는 다양한 주사요법이 있는 점과 보트리엔트의 건강보험급여 적용으로 대체 약제 활용 가능성이 있음을 이유로 들었다.
사회적 요구가 높던 엔허투와 욘델리스의 암질심 통과에 따라 큰 이변이 없는 한 급여 포함까지는 순조롭게 이어질 것으로 보인다.
한편 건강보험 요양급여의 기준에 관한 규칙 제5조 및 제5조의2”에 의해 심평원장은 중증질환자에게 처방‧투여하는 약제 중 복지부장관이 정해 고시하는 약제에 대해 요양급여의 적용기준 및 방법에 관한 세부사항을 중증질환심의위원회 심의를 거쳐 공고할 수 있다.
?????? 3 ( ) .
3 ( ) .
.
.
3 .
, .
HER2 HER2 .
HER2 HER-2 .
.
. , , .
, .
.

,
.
HER2 2 HER2 .
5 .
15 .
() 1% .
2021 6 , .
.
5 52 .

