
 디지털치료제기기에 대한 급여가 임박함에 따라 국내에서도 상용화를 위한 시도가 점차 늘어나고 있는 추세인 것으로 나타났다.
디지털치료제기기에 대한 급여가 임박함에 따라 국내에서도 상용화를 위한 시도가 점차 늘어나고 있는 추세인 것으로 나타났다.
2019년 식약처가 1건의 디지털치료기기 임상을 허가한 이후 올해에는 15건의 신규 임상을 승인했다.
16일 식약처에 따르면, 국내에서 디지털치료기기를 상용화하기 위한 임상이 현재까지 총 25건이 허가됐다.
디지털치료기는 의약품이 아니면서 의약품과 같이 질병을 치료하고 건강을 개선하는데 사용하는 소프트웨어(SW) 의료기기를 뜻한다.
흔히 디지털치료제라고 불리기도 하지만 정식 명칭은 디지털치료기기다. 식약처는 디지털치료기기를 의료기기로 분류하고 있으며, 정식 상용화를 위해서는 임상을 진행해야 한다.
그동안 국내에서 디지털치료기기를 일부 병원에서 상용화하기도 했으나, 식약처가 허가한 임상을 바탕으로 허가받은 제품이 아니기 때문에 아직까지 국내 1호 디지털치료기기는 없는 상태다.
하지만 조만간 국내에서도 디지털치료기기 승인이 이뤄질 것으로 전망된다. 2019년부터 임상이 본격화되면서 국내 업체들이 임상을 마무리하고 허가를 준비하고 있기 때문이다.
최근에는 디지털치료기기에 대한 급여 기준이 정해지면서 점차 상업화를 시도하는 업체들도 늘어나고 있다.
2019년에 1건에 불과했던 임상이 2021년에는 9건으로 늘었으며, 올해에는 15건의 신규 임상이 승인됐다.
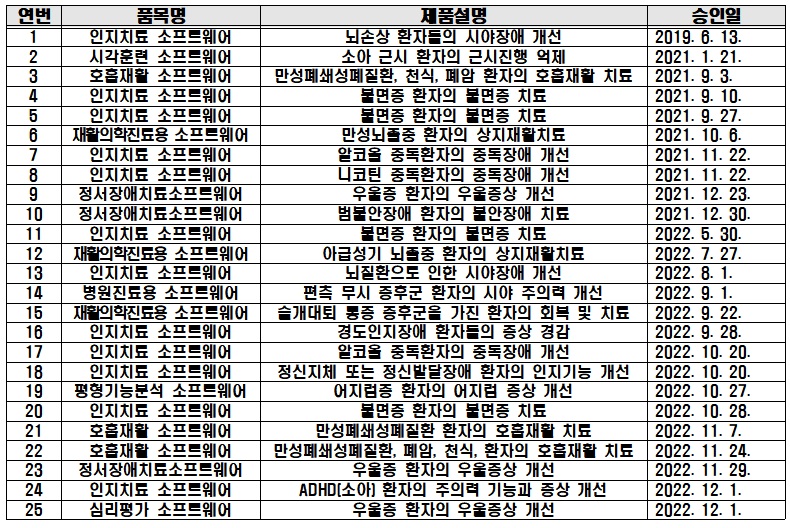
또 재활의학진료용 소프트웨어와 정서장애치료 소프트웨어, 호흡재활 소프트웨어가 각각 3건, 평형기능분석 소프트웨어·병원진료용 소프트웨어·시각훈련 소프트웨어·심리평가 소프트웨어 등이 각각 1건이다.
용도는 비교적 다양한 질환 치료에 활용되고 있다. 불면증 치료, 알코올 중독장애 개선, 니코틴 중독장애 개선, 경도인지장애 증상 개선, ADHD 환자 주의력 기능과 증상 개선 등이 대표적이다.
주로 정신신경계 질환에 사용되고 있으나, 호흡재활 치료나 상지재활 치료, 시야 장애 개선 등에 초점을 맞춰 개발하는 제품도 있다.
디지털치료기기 임상의 경우 의약품과 달리 임상 기간이 길지 않기 떄문에 일부 업체는 이미 임상을 마치고 품목 허가 단계에 있는 것으로 알려졌다.
이에 따라 늦어도 내년에는 국내서 1호 디지털치료기기 허가와 함께 의료 현장에서 상용화가 가능할 것으로 전망된다.
