
 연간 700억원대 셀트리온제약 대표 품목인 고덱스가 퇴출 가능성이 또 다시 제기됐으나, 급여 유지하는 것으로 결론났다.
연간 700억원대 셀트리온제약 대표 품목인 고덱스가 퇴출 가능성이 또 다시 제기됐으나, 급여 유지하는 것으로 결론났다.
최종 관문으로 여겨졌던 건정심 회의는 사실상 급여 퇴출을 논의하는 자리도 아니었던 것으로 알려졌다.
지난 22일 보건복지부 건강보험정책심의위원회에서는 2022년 급여적정성 재평가 결과 보고 추가안건에서 고덱스 재심의 과정을 보고했다.
지난달 열린 건정심에서 위원들은 임상적 유용성이 불문명한 약제인 고덱스의 평가 방식에 문제를 제기하면서 퇴출 가능성이 제기됐었다.
하지만 이번 건정심에서 고덱스 퇴출을 결정짓는 자리가 아닌 급여유지 과정을 설명하는 수준에서 회의가 진행됐다.
그 과정을 보면, 고덱스는 지난 7월 급여적정성 재평가 결과에서 급여 퇴출이 결정됐다. 당시 임상적 유용성이 불문명한 상태에서 비용 효과성이 충분치 않다는 이유였다.
하지만 지난 10월 결과는 정반대가 됐다. 임상적 유용성은 불문명하지만, 회사 측의 자진 약가로 인해 비용효과성이 인정되고, 사회적 요구도가 높다고 판단됐기 때문이다.
지난 건정심에서 임상적 유용성이 불문명한 약제가 약가 인하 조건으로 급여를 유지시키는 것에 대한 의문을 제기한 바 있다.
하지만 복지부는 급여적정성 재평가 과정을 설명하며, 고덱스가 급여 유지된 이유를 설명했다.
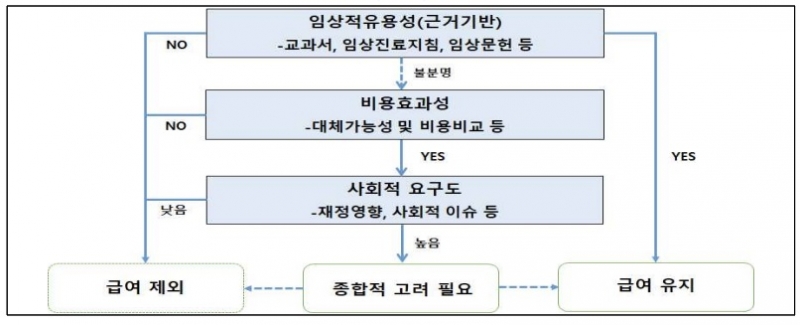 임상적 유용성이 인정될 경우, 비용효과성이나 사회적 요구도에 상관없이 급여는 유지된다. 임상적 유용성이 미흡하면 급여 퇴출된다.
임상적 유용성이 인정될 경우, 비용효과성이나 사회적 요구도에 상관없이 급여는 유지된다. 임상적 유용성이 미흡하면 급여 퇴출된다.
하지만 임상적 유용성이 불분명할 약제의 평가 과정은 상이하다. 이들 약제는 비용 효과성을 우선 평가, 효과성이 있다고 판단한 뒤 다음 단계인 사회적 요구도까지 인정될 경우에 급여가 유지된다.
이는 임상적 유용성 불문명이 임상적 미흡과는 다른 의미이기 때문이다. 실제 고덱스의 경우 임상적 유용성에 있어 교과서·임상진료지침·HTA 보고서에는 언급이 없어 확실한 인정 요건을 가진건 아니나, SCIE급 임상연구문헌 3편에서 임상 효과가 인정되고 있다.
이에 따라 고덱스는 복지부가 규정해 놓은 급여적정성 재평가 과정을 거쳐 급여가 유지된 것이다.
하지만 건강약사회를위한약사회를 비롯한 시민단체는 이 같은 평가 과정에 대해 불만을 제기하고 있다.
건약은 "11월 건정심에서는 다음에 다시 재평가를 논의하기로 했는데, 12월 건정심에서 재평가 논의를 단순 보고로 종결한 것은 보건복지부가 지난 11월 회의 결과를 스스로 부정한 것이나 다름없다"고 밝혔다.
이어 "12월 건정심에서 급여적정성 재평가를 보고 안건으로 처리한 보건복지부는 분명하게 해명해야 한다"고 지적했다.
