
 식품의약품안전처가 2018년부터 2021년까지 2만8857개 품목에 대한 갱신을 진행했고, 이중 1만1396개 품목(39%)이 정리됐다.
식품의약품안전처가 2018년부터 2021년까지 2만8857개 품목에 대한 갱신을 진행했고, 이중 1만1396개 품목(39%)이 정리됐다.
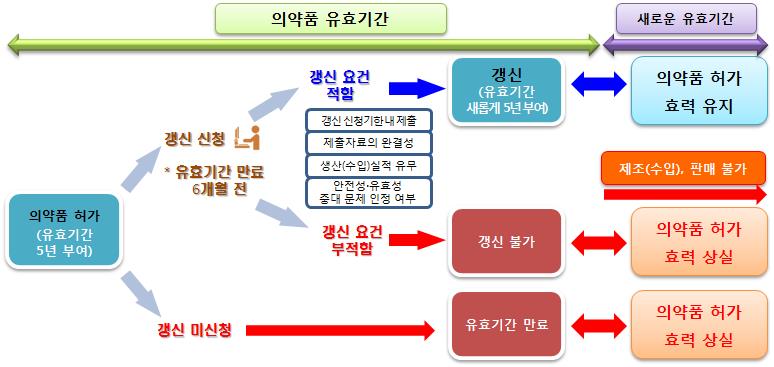
8일 식약처(처장 오유경)는 허가·신고된 의약품의 유효기간(5년)을 품목별로 부여해 안전성과 효과성을 주기적으로 확보하고 효율적으로 관리하기 위한 ‘의약품 품목갱신 제도’ 제2주기(2023~2027년) 운영 방안을 공개했다.
의약품 품목갱신 제도는 2018년부터 본격 시행됐으며, 5년 주기로 안전관리자료, 외국사용 현황, 품질관리자료, 제조 및 수입 실적 등을 재검토하는 것을 골자로 한다.
식약처는 허가‧신고됐으나 제조‧수입되지 않아 서류상으로만 존재하는 의약품을 삭제함으로써 실제 유통 중인 품목의 의약품 안전관리에 집중할 수 있는 기반을 마련했다.
실제 2018년부터 2021년까지 2만8857개 품목에 대한 갱신이 진행돼 이 중 1만1396개 품목(39%)이 유효기간 만료 등으로 정리됐다.
같은 기간 ‘아스피린제제(진통제)’ 등 105개 성분(2265개 품목)의 효능·효과, 용법·용량 등 허가·신고사항을 개선해 보다 안전하고 효과적인 의약품 사용 환경을 조성했다.
2주기에선 ➊모든 전문의약품 부작용 분석‧평가자료 제출 ➋유효성 인정 범위 및 검토 절차 개선 ➌제품 품질평가 자료를 제조‧수입자 준수사항과 일치 ❹표시기재 확인·관리 강화 ❺제조원별·포장단위별 제조·수입실적 세부 검토 등이 포함된다.
특히 안전관리책임자의 부작용 분석‧평가 자료는 그간 한국의약품안전관리원에 보고한 자료가 없는 경우 제출했으나, 앞으로는 규정을 개정해 모든 전문의약품에 대해 제출받아 심사한다.
유효성 입증자료로 기존에는 주요 국가 허가사항 또는 허가 규정에 적합한 임상시험자료만 인정했지만 제2주기부터는 인정 범위가 임상 연구문헌(범주 1, 2)까지 확대된다.
희귀의약품 등에 대해서는 유효성을 입증하기 위해 제출할 수 있는 자료 범위를 범주 3의 임상 연구문헌 또는 의학회 추천 교과서·임상진료지침까지 인정키로 했다.
식약처는 내년부턴 본부에서 훈련된 역량 있는 심사원들이 각 지방청으로 배치돼 지방청 관할 허가·신고 품목에 대해 갱신 심사해 기관별 역량과 환경을 지속적으로 확보·개선할 계획이다.
식약처 관계자는 "의약품 품목갱신 제도 제2주기 시행으로 유통·판매 중인 의약품에 대한 최신의 안전성과 효과성을 주기적 확보함으로써 국내 의약품 안전관리 수준 향상과 국민 건강 보호에 도움이 될 것으로 기대한다"고 설명했다.
