
[데일리메디 박근빈 기자] 생산·수입·공급이 중단될 시 필수적으로 보고를 해야하는 의약품은 252개 제약사, 1933품목으로 정해졌다. 해당 품목을 보유한 제약사는 공급 중단일 60일 전에 사전보고가 이뤄져야 한다.
최근 건강보험심사평가원(원장 김승택) 의약품관리종합정보센터는 2018년도 생산·수입·공급 중단 보고대상 의약품 1933품목(252개 제약사)을 공고했다.
생산·수입·공급 중단 보고대상 의약품은 제조·수입사가 생산·수입 및 공급을 중단하는 경우 그 사유를 식품의약품안전처장에게 보고해야 하는 완제 의약품을 말한다.
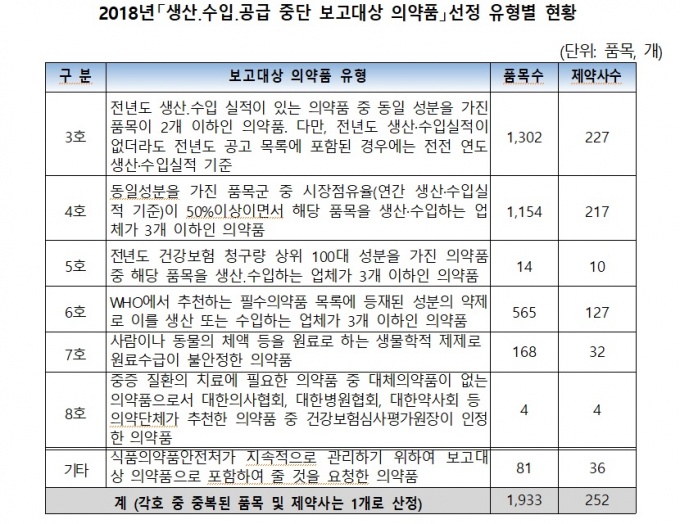
이는 총 8개 유형으로 구분되며 생산·수입·공급 중단 보고대상 의약품 고시 제2조(보고대상의약품)에 근거를 두고 있다.
심평원은 8개 유형 중 퇴장방지의약품과 희귀의약품을 제외한 6개 유형에 대해 전년도 생산·수입 실적과 건강보험 청구실적 및 의약단체, 업계 의견 등을 반영해 해당 완제 의약품을 선정하고 복지부장관의 승인을 받아 공고하고 있다.
대상 품목은 ▲일동제약 블루케어스프레이(수용성아줄렌) ▲하나제약 덴티스타캡슐(독시사이클린하이클레이트수화물) ▲녹십자 페리덱스연고(덱사메타손) ▲한미약품 히아로겔(히알루론산나트륨) ▲일약약품 노루모현탁액 ▲삼진제약 위튼겔(보에마이트) 등이 선정됐다.
2018년 선정된 1933품목 중 ‘전년도 생산·수입 실적이 있는 의약품 중 동일성분 의약품이 2개 이하인 의약품’이 1302개(227개 제약사)로 가장 많았다.
또한 의약품 목록에는 식약처에서 국가필수의약품 등 지속적으로 관리가 필요해 보고대상 의약품으로 선정해 달라고 요청한 81품목(36개 제약사)도 포함됐다.
제조·수입사가 생산·수입·공급 중단 보고대상 의약품의 생산·수입 또는 공급을 중단하는 경우‘의약품 등의 안전에 관한 규칙’에 따라 중단일의 60일 전까지 그 사유를 식약처장에게 보고해야 하며, 이를 준수하지 않을 경우 업무정지 처분을 받게 된다.
심평원 정동극 의약품관리종합정보센터장은 “생산․수입․공급 중단 보고대상 의약품 공고는 의약품 공급부족을 사전에 예방하고 의약품의 원활한 수급관리를 유도하여 환자 진료의 차질을 방지하는 효과가 있다”고 밝혔다.
이어 “해당 의약품을 생산 및 수입하는 제약사, 관련 단체는 제도가 원활하게 운영될 수 있도록 적극 협조해주길 바란다”고 당부했다.
