
 한독이 국내 독점 판매 권한을 보유한 급성골수성백혈병 치료제 '빅시오스(다우노루비신/시타라빈)'가 약제급여평가위원회의 심의를 통과했다.
한독이 국내 독점 판매 권한을 보유한 급성골수성백혈병 치료제 '빅시오스(다우노루비신/시타라빈)'가 약제급여평가위원회의 심의를 통과했다.
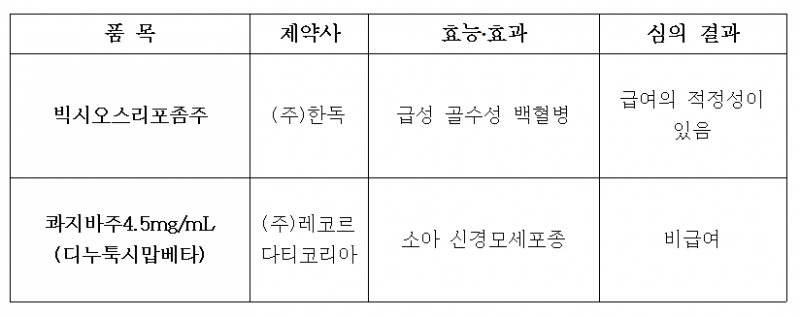
빅시오스는 글로벌 바이오 제약회사 재즈 파마슈티컬이 개발한 신약으로 이번 심의에서 급여 적정성이 적합하다는 평가를 얻어냈다.
건강보험심사평가원은 8일 제8차 약제급여평가위원회를 열고 결정신청 약제의 요양급여 적정성에 대해 심의 결과를 발표했다.
위원회는 빅시오스에 대해 급여 적정성이 있다고 판단했다. 빅시오스는 새로 진단받은 치료 관련 급성 골수성 백혈병(t-AML) 또는 골수이형성증 관련 변화를 동반하는 급성 골수성 백혈병(AML-MRC) 환자의 치료를 주요 혜택으로 한다.
반면, 레코르다티코리아가 신청한 소아 신경모세포종 치료제 '콰지바주(디누툭시맙베타)'는 비급여로 결정됐다.
한편, 심평원은 혁신신약 가치 보상과 환자 접근성 확대를 위해 약가 제도를 개선키 위해 약평위 논의를 거쳐 신약 등 협상대상 약제의 세부평가기준을 개정했다.
질병 부담이 큰 중증 난치질환에 사용되는 약제에 대해 위험분담제 적용 대상을 확대하고 추가 청구액이 15억원 미만인 위험분담 약제의 급여 확대 절차를 간소화했다.
또 ICER 임계값 평가에 있어 혁신성 의미를 구체화하고 성과기반 환급형 위험분담 약제의 임상성과 평가 절차를 명확화해서 신약의 적정 가치를 반영하는 기준을 마련했다.
심평원은 “제약사는 결과 통보 후 30일 이내 건강보험심사평가원에 재평가를 신청할 수 있으며 제출된 내용은 약제급여평가위원회의 재심의를 거치게 된다”고 밝혔다.
