

중증 치매인 알츠하이머병을 유발하는 독성 단백질이 국내 연구진에 의해 발굴됐다.
카이스트(총장 이광형)는 "화학과 임미희 교수(금속신경단백질연구단 단장) 연구팀이 알츠하이머병 관련 새로운 병리적 네트워크를 제시했다"고 20일 밝혔다.
연구팀은 한국기초과학지원연구원(원장 양성광) 바이오융합연구부 이영호 박사 연구팀, KAIST 화학과 백무현 교수 연구팀, 의과학대학원 한진주 교수 연구팀과 공동 연구하고, 한국생명공학연구원(원장 김장성) 희귀난치질환연구센터 이다용 박사 연구팀도 참여했다.
학계에 따르면 알츠하이머병 환자들의 뇌에서 대표적으로 나타나는 병리적 현상은 노인성 반점 축적이다.
노인성 반점의 주된 구성분은 아밀로이드-베타 펩타이드로인 응집체로 세포 내 물질들과 결합해 세포 손상을 유발한다. 이에 이들 응집체와 세포 사멸 간의 상관관계가 활발히 연구되고 있다.
그러나 아밀로이드-베타와 세포 사멸 유발 인자들 간 직접적인 상호작용에 대해서는 아직 많은 부분이 밝혀진 바 없다.
‘아두카누맙’ 등 최근 미국식품의약국(FDA)이 승인한 알츠하이머병 신약은 아밀로이드-베타 펩타이드 응집체의 세포 손상을 주요 타깃으로 한다.
그러나 부작용 등으로 사용이 제한되고 있어 신약 개발 방향 전환 및 개선이 필요함을 연구자들은 절실히 느끼고 있었다는 설명이다.
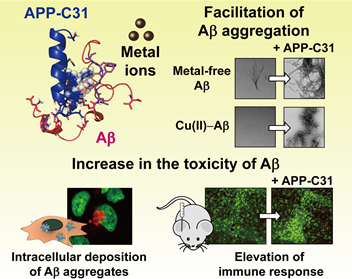 이번에 임미희 교수 연구팀은 알츠하이머병에서 과발현되고 신경세포 사멸을 유발하는 ‘아밀로이드 전구체 C 말단 절단체’ 단백질이 아밀로이드-베타 및 금속-아밀로이드-베타 복합체와 결합해 응집을 촉진하고, 독성 촉진제 역할을 한다는 것을 세계 최초로 증명하는 연구를 내놨다.
이번에 임미희 교수 연구팀은 알츠하이머병에서 과발현되고 신경세포 사멸을 유발하는 ‘아밀로이드 전구체 C 말단 절단체’ 단백질이 아밀로이드-베타 및 금속-아밀로이드-베타 복합체와 결합해 응집을 촉진하고, 독성 촉진제 역할을 한다는 것을 세계 최초로 증명하는 연구를 내놨다.
그동안 세포사멸 인자로만 알려져 있고, 그 메커니즘이 정확히 규명되지 않았던 아밀로이드 전구체 C 말단 절단체 단백질과 알츠하이머병 병리 인자들 간의 직접적 상호작용을 최초로 확인한 것이다.
임미희 교수는 “아밀로이드 전구체 C 말단 절단체 자체 또는 아밀로이드-베타과 결합한 복합체가 알츠하이머병의 새로운 바이오마커로 작용할 수 있고, 또한 그들이 새로운 신약개발 타깃이 될 수 있다”고 의의를 밝혔다.
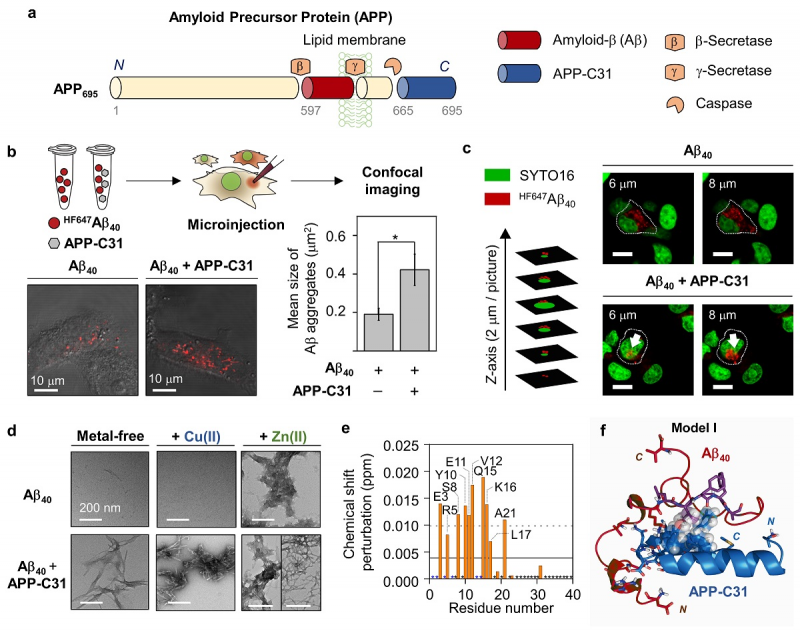 연구팀의 남은주 박사(KAIST 화학과 박사 졸업, 現 브리검 여성 병원 및 하버드 의과대학 연구원)가 제1 저자로 참여한 이번 연구는 세포 내 단백질 미세주입 기술을 통해 세포 안에서 아밀로이드 전구체 C 말단 절단체가 아밀로이드-베타 응집 촉진에 미치는 역할도 확인했다.
연구팀의 남은주 박사(KAIST 화학과 박사 졸업, 現 브리검 여성 병원 및 하버드 의과대학 연구원)가 제1 저자로 참여한 이번 연구는 세포 내 단백질 미세주입 기술을 통해 세포 안에서 아밀로이드 전구체 C 말단 절단체가 아밀로이드-베타 응집 촉진에 미치는 역할도 확인했다.
나아가 뉴런 세포 및 설치류의 뇌에서 아밀로이드-베타와 관련된 세포 사멸, 뉴런 손상, 염증반응이 아밀로이드 전구체 C 말단 절단체에 의해 더욱 증가하는 현상도 최초로 확인했다.
이번 연구는 국제 저명 학술지인 ‘어드밴스드 사이언스(Advanced Science, Impact factor: 15.1)’에 11월 10일자로 게재됐다.
