
[데일리메디 양보혜 기자] 올해 하반기부터 제네릭 의약품 가격 제도가 현행 '동일제제-동일가격' 원칙에서 제네릭 개발 노력에 따른 '차등가격' 원칙으로 개편된다.
자체 생물학적동등성 시험 실시와 등록 원료의약품(DMF) 사용 등 2개 기준을 얼마나 충족하느냐에 따라 제네릭 약가가 달리 산정된다. 단, 1개 성분에 20번째까지 건강보험 등재 제네릭에 한해서만 새 기준이 적용된다.
보건복지부(장관 박능후)는 27일 이 같은 내용을 담은 “제네릭(복제약) 의약품 약가제도 개편방안”을 전격 발표했다.
복지부 측은 "이번 개편안은 2018년 발사르탄 사태를 계기로 제네릭 제도 전반에 대한 개편이 필요하다는 판단에 따라 마련됐다"며 "식약처가 지난 2월 발표한 '허가제도 개편 방향' 등과 연계해 추진된다"고 설명했다.
구체적으로 보면 의약품 성분별 일정 갯수 내(20개)에서는 급여 등재 순서와 상관 없이 2개 기준 요건 충족 여부에 따라 제네릭 가격이 정해진다. 자체 생동 실시, 등록된 원료의약품 사용 등이 기준이다.
자체 생동 인정 범위는 제약사가 단독으로 실시하거나, 공동 실시 때 주관업체인 경우에는 자체 생동을 한 것으로 인정한다.
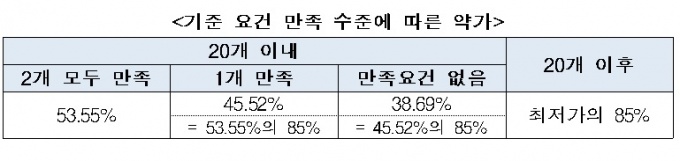
2개 기준 요건을 모두 충족하면 현재와 같이 오리지널 의약품 가격의 53.55%로 가격이 산정된다. 1개, 0개 등 기준 요건 충족 수준에 따라서 53.55%에서 0.85씩 각 각 곱한 가격으로 산정된다.
그러나 급여 등재 순서 21번째부터는 기준 요건 충족 여부와 상관없이 최저가의 85% 수준으로 약가를 정한다. 21번째 제네릭은 20개 내 제품 최저가의 85%, 22번째 제네릭은 21번째 제네릭 가격의 85%로 결정된다.
기존에 등재된 제네릭에는 개수 제한은 적용되지 않고 기준 요건 충족 수준에 따란 가격 차등 방안만 적용될 예정이다.
복지부 측은 "제네릭 내에서 등재 순서 20번째까지의 제품군 청구액 비중이 90%인 점 등을 고려했다"고 전했다.
이번 제네릭 의약품 약가제도 개편안은 '약제의 결정 및 조정기준' 규정 개정을 거쳐 이르면 금년 하반기부터 시행할 예정이다.
단, 제약계 및 의료 현장의 혼란을 최소화하기 위해 신규 제네릭과 기존에 등재된 제네릭(현재 건강보험 급여 적용 중인 제네릭)으로 구분해 적용 시점을 다르게 할 계획이다.
신규 제네릭의 경우, 규정 개정 및 일정 기간 경과 후 급여를 신청하는 제품부터 개편안을 적용한다. 이미 급여 등재된 제네릭은 기준 요건 적용 준비에 소요되는 기간을 고려해 준비기간을(3년) 부여한 후 적용한다.
제네릭 중 저가의약품 및 희귀의약품, 퇴장방지의약품 등은 관련 규정에 따라 개편안 적용 대상에서 제외된다.
곽명섭 복지부 보험약제과장은 "이번 개편안 시행을 통해 제약사의 제네릭 의약품에 대한 책임성을 높이고 대내외 경쟁력도 강화되도록 하는 한편, 환자 안전 관리 강화 등에도 긍정적인 영향을 미칠 것으로 기대한다"고 말했다.
이어 곽 과장은 "세부 운영 방안에 대해서는 제약계와 지속적인 논의를 통해 제약사, 요양기관(병의원과 약국) 및 환자들 불편이 없도록 세심히 살펴가며 추진하겠다"고 덧붙였다.
