
 국산 신약 31호인 유한양행 렉라자(성분명 레이저티닙)가 급여기준 확대에 성공하며 건강보험 급여화를 위한 첫 관문을 통과했다.
국산 신약 31호인 유한양행 렉라자(성분명 레이저티닙)가 급여기준 확대에 성공하며 건강보험 급여화를 위한 첫 관문을 통과했다.
주요 효능‧효과는 EGFR 엑손 19 결손 또는 엑손 21(L858R) 치환 변이된 국소진행성 또는 전이성 비소세포폐암 환자의 1차 치료다.
렉라자의 경우 아스트라제네카의 타그리소(오시머티닙)과 EGFR 돌연변이 양성 비소세포폐암 1차 치료제 시장 선점을 위한 열띤 경쟁 중인 만큼 경쟁에 청신호가 켜졌다는 평이다.
30일 건강보험심사평가원(원장 강중구)은 2023년 제6차 암질환심의위원회에서 심의한 ‘암환자에게 사용되는 약제에 대한 급여기준 심의결과’를 공개했다.
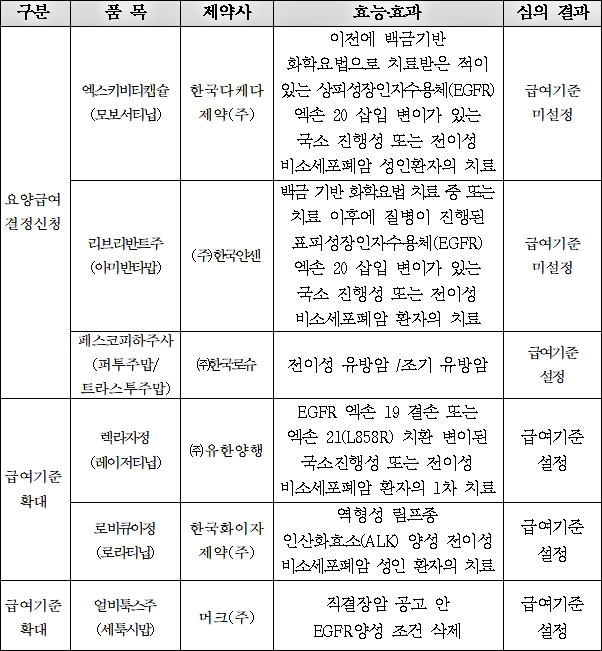
이번 평가에서는 급여기준 확대 3건과 요양급여 결정신청 3건 등 총 6건을 심사했다.
렉라자 외에도 한국화이자제약의 로비큐아정(로라티닙)도 역형성 림프종 인산화효소(ALK) 양성 전이성 비소세포폐암 성인 환자 치료에 대한 급여기준이 설정됐다.
또 머크의 얼비툭스주(세툭시맙)는 직결장암 공고 안 EGFR양성 조건 삭제로 급여기준이 설정됐다.
요양급여 결정신청의 경우 3건 중 1건만 급여기준이 설정됐다. 주인공은 한국로슈 페스코피하주사(퍼투주맙/트라스투주맙)이다. 주요 효능 ‧효과는 전이성 유방암‧조기 유방암이다.
한국다케다 엑스키비티캡슐·한국얀센 리브리반트주 통과 못해
반면 한국다케다의 엑스키비티캡슐(모보서티닙)과 한국얀센의 리브리반트주(아미반타맙)은 급여 허들을 통과하지 못했다.
엑스키비티캡슐의 경우 주효과로 백금기반 화학요법으로 치료받은 적이 있는 상피성장인자수용체(EGFR) 엑손 20 삽입 변이가 있는 국소 진행성 또는 전이성 비소세포폐암 성인환자의 치료로 신청했다.
리브리반트주는 백금 기반 화학요법 치료 중 또는 치료 이후에 질병이 진행된 표피성장인자수용체(EGFR) 엑손 20 삽입 변이가 있는 국소 진행성 또는 전이성 비소세포폐암 환자의 치료다.
심평원은 "해당 약제의 급여기준은 식품의약품안전처 허가사항의 효능‧효과 범위 내에서 임상문헌, 국내 및 외국 가이드라인, 전문가 의견에 따라 다르게 설정될 수 있다"고 밝혔다.
