[데일리메디 양보혜 기자] 엠지의 수액주사제 2품목, 한미약품의 항생제 1품목이 판매중지 및 회수·폐기 조치된다.
식품의약품안전처(처장 이의경)는 엠지가 제조한 ‘엠지티엔에이주페리’ 등 수액주사제 2개 품목에서 품질 부적합이 확인된 4개 제조번호에 대해 잠정 판매·사용중지하고 회수 조치한다고 19일 밝혔다.
이번에 확인된 엔도톡신은 세균의 세포벽에 있는 물질로, 0.5EU/ml를 상회할 경우 발열을 유발한다.
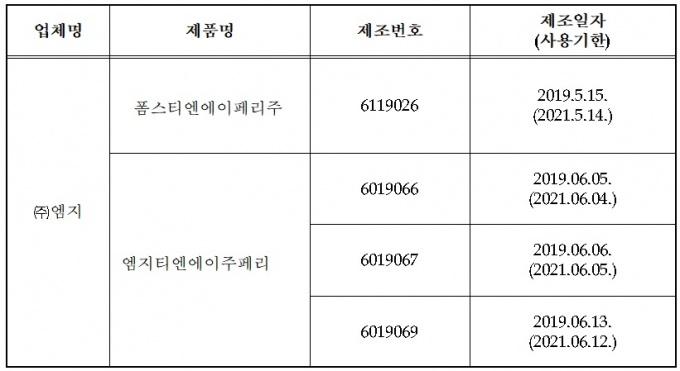
대상 품목은 엠지가 제조한 ‘폼스티엔에이페리주’(1개 제조번호), ‘엠지티엔에이주페리’(3개 제조번호) 영양수액제다.
식약처는 "엠지를 대상으로 제조‧품질관리 기준(GMP) 준수 여부 등 전반에 대해 조사하고 있으며, 관련 규정 위반이 확인되는 경우 행정처분 등의 조치를 취할 예정"이라고 밝혔다.
이어 "원인 조사를 위해 해당 공장에서 생산돼 유통되고 있는 의약품 중 영향이 있을 것으로 예측되는 제품을 수거해 검사도 함께 진행할 예정"이라고 덧붙였다.
식약처는 의‧약사 등 전문가에게 해당 제품을 대체 치료제로 전환하고, 제품 회수가 이뤄질 수 있도록 협조 요청하는 안정성 서한을 배포했다. 복지부 및 심평원에는 해당 2개 제품에 대한 처방 제한을 요청했다.
앞서 한미약품의 항생제 '한미세포탁심나트륨주사500mg' 역시 판매중지 및 회수·폐기 처분이 내려졌다. 회수 조치 이유는 주사제 내 이물질 혼입 우려다.
대상 제품은 지난해 10월 18일, 29일, 23일 제조된 '109718011', '109718021', '109718031'과 올해 2월 27일 3월 7일 제조된 '109718031', '109719011' 등 총 5개다.

 이번에 확인된 엔도톡신은 세균의 세포벽에 있는 물질로, 0.5EU/ml를 상회할 경우 발열을 유발한다.
이번에 확인된 엔도톡신은 세균의 세포벽에 있는 물질로, 0.5EU/ml를 상회할 경우 발열을 유발한다. 