[데일리메디 한해진 기자] 실제 인간 신장(콩팥)과 매우 유사한 고도로 분화된 신장 오가노이드가 개발돼 신장병 연구 및 치료제 개발이 진일보할 전망이다.
가톨릭대학교 성빈센트병원은 신장내과 김용균 교수팀(가톨릭대학교 의과대학 세포사멸질환 연구센터, (주)알젠오가노 바이오테크놀로지)과 포항공대 조동우 교수팀, 광주과학기술원 박지환 교수팀이 공동으로 기존의 신장 오가노이드의 제한점을 극복한 신장 오가노이드 분화 개발에 성공했다고 밝혔다.
‘미니 신장’이라고도 불리는 신장 오가노이드는 줄기세포에서 분화돼 실제 인간의 신장을 구성하는 세포들로 구성되고 기능을 하는 3차원 세포 구조체로, 차세대 신약 개발 및 재생치료 핵심 요소 중 하나다.
기존의 신장 오가노이드는 해외에서 개발된 프로토콜로 제작됐다. 오가노이드 내 혈관 형성이 5% 정도로 매우 제한적이고, 세포 성숙도 역시 인간의 신장과 비교해 미성숙한 상태다.
또한 오가노이드 내 신장이 아닌 세포들(off-target 세포)이 10% 정도 존재, 실제 임상 치료 및 의료산업 현장에 서 사용하는 데는 한계가 있었다.
이에 연구팀은 실제 인간의 신장 발생 과정에 대한 깊은 이해를 바탕으로 고도분화 신장 오가노이드 분화 프로토콜 개발에 나섰다.
신장 세포외 기질의 미세 환경이 신장 발생에 중요한 역할을 한다는 사실에 착안해 포유동물 신장을 탈세포화 한 후 세포외 기질을 추출해 세포 배양접시에 코팅했다.
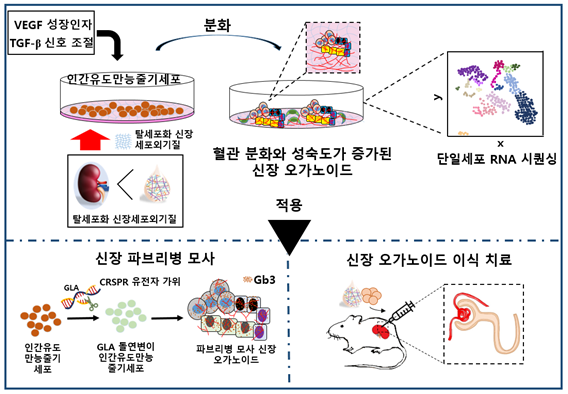
이어 인간 신장 사구체 및 혈관 발생에 중요한 역할을 하는 TGF-β 신호를 조절하고, VEGF 성장인자를 정교하게 혼합 구성해서 ‘신장 오가노이드 고도분화 프로토콜’을 개발했다.
국내 기술로 개발된 고도분화 신장 오가노이드는 기존 해외 프로토콜을 활용한 신장 오가노이드에 비해 혈관 내피세포 증식이 항진돼 오가노이드 내 혈관망을 형성하고, 사구체 내로 혈관이 침투해 신장 여과 기능에 필수적인 구조물인 여과장벽이 형성돼 있다.
또 신장 오가노이드의 근위세뇨관 세포 성숙도와 포도당 재흡수 기능이 향상됐으며, 신장 오가노이드 내 off-target 세포들이 감소됐다.
이와 함께 연구팀은 CRSPR-Cas9 유전자 편집기술을 이용해 난치성 신장질환인 파브리병의 원인 유전자 갈락토시데이즈-알파의 돌연변이를 유도하고, 이를 이번에 개발한 고도분화 프로토콜을 이용해 신장 오가노이드로 분화시켜 실제 인간의 파브리병과 같이 신장 및 혈관의 병리학적인 병변을 만드는데 성공했다.
더불어 신장 오가노이드를 탈세포화 된 세포외 기질과 함께 쥐의 신장에 이식하면 생착이 잘 되고 이식 효과가 증진된다는 사실도 이번 연구를 통해 증명했다.
성빈센트병원 김용균 교수는 “이번 연구는 국내 기술로서 기존에 해외에서 개발된 신장 오가노이드 한계를 극복하고, 성숙도 및 기능이 한 층 더 향상된 신장 오가노이드 제작하는데 성공했으며, 나아가 이를 이용해 신장 질환 모사 및 재생치료 가능성을 증명했다는데 의의가 있다”며 “연구팀이 개발한 고도분화 신장 오가노이드가 향후 추가 연구를 거쳐 실제 임상 치료 및 의료 현장에 사용되길 기대한다”고 강조했다.
한편 이번 연구 성과는 'Advanced Science (인용지수: 16.806)' 최신호에 게재됐다.