
한국화이자제약 보술리프정이 2개 적응증 가운데 1개만 급여기준을 통과, 절반의 성공을 거뒀다.
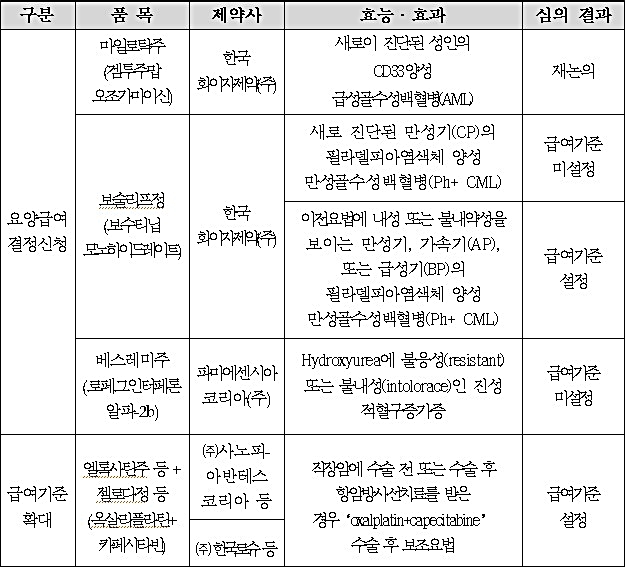
새로 진단된 만성기(CP) 필라델피아염색체 양성 만성골수성백혈병(Ph+ CML)은 급여기준이 미설정됐다. 반면 이전요법에 내성 또는 불내약성을 보이는 만성기, 가속기(AP), 또는 급성기(BP) 필라델피아염색체 양성 만성골수성백혈병(Ph+ CML)은 급여 기준을 인정받았다.
또 함께 암질환심의위원회 심의 대상이 됐던 급성골수성백혈병(AML) 치료제 마일로탁주 역시 심의 결과, 재논의가 필요한 것으로 결론났다.
27일 건강보험심사평가원(원장 강중구)은 2023년 제5차 암질환심의위원회에서 심의된 ‘암환자에게 사용되는 약제 급여기준 심의결과’를 공개했다.
먼저 사노피와 한국로슈 엘록사틴주와 젤로다정 등은 각각 급여기준 확대에 성공했다.
두 치료제 모두 직장암에 수술 전 또는 수술 후 항암방사선치료를 받은 경우‘oxalplatin+capecitabine’ 수술 후 보조요법에 사용되는 동일한 적응증을 갖고 있다.
반면 파마에센시아코리아의 베스레미주는 급여권 편입 여정에 실패했다.
베스레미주는 Hydroxyurea에 불응성(resistant) 또는 불내성(intolorace)인 진성 적혈구증가를 적응증으로 한다.
한국화이자제약 보술리프정이 2 1 , .
(CP) (Ph+ CML) . , (AP), (BP) (Ph+ CML) .
(AML) , .
27 ( ) 2023 5 .
.
oxalplatin+capecitabine .
.
Hydroxyurea (resistant) (intolorace) .


